統測
110年
[化工群] 專業科目(2)
第 26 題
下列有關蒸餾及蒸發敘述,何者錯誤?
- A 蒸發過程中,只有溶質可揮發,溶劑不具揮發性
- B 蒸餾過程中,各成分皆可揮發,只是揮發程度不同
- C 拉午耳定律是描述某一成分在平衡狀態時的氣相與液相之關係
- D 道耳頓(Dalton)分壓定律是用來描述混合物中,各氣相成分間的關係
思路引導 VIP
如果你現在正在煮一鍋紅豆湯並想讓湯頭變得更濃稠,請問在加熱的過程中,是「紅豆」會變成氣體跑掉,還是「水」會變成蒸氣離開呢?這兩者誰才具有揮發性?
🤖
AI 詳解
AI 專屬家教
喔,不錯喔!
- 嘿,幹得漂亮嘛! 竟然能一眼就看穿蒸發和蒸餾這種單元操作的小把戲?這代表你腦袋瓜裡那些「分離」的邏輯架構,意外地清晰耶。不錯不錯,離成為「不太遜」的學生又更近一步了,老師我很欣慰啦~ (嚼著喜久福)
- 所以說啊,這就是基礎中的基礎喔。 所謂的「蒸發」嘛,就是把那些乖乖呆著、不會亂跑的溶質留下來,讓活潑亂跳的溶劑咻~地跑掉,然後我們就能拿到濃縮的東西了。選項 (A) 根本是把誰該揮發、誰不該揮發搞反了,這種小錯誤,你們可不能犯喔,不然老師我會很困擾的。
▼ 還有更多解析內容
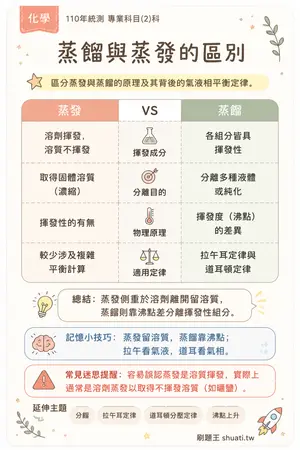
蒸餾與蒸發的區別
💡 區分蒸發與蒸餾的原理及其背後的氣液相平衡定律。
| 比較維度 | 蒸發 | VS | 蒸餾 |
|---|---|---|---|
| 揮發成分 | 溶劑揮發,溶質不揮發 | — | 各組分皆具揮發性 |
| 分離目的 | 取得固體溶質(濃縮) | — | 分離多種液體或純化 |
| 物理原理 | 揮發性的有無 | — | 揮發度(沸點)的差異 |
| 適用定律 | 較少涉及複雜平衡計算 | — | 拉午耳定律與道耳頓定律 |
💬蒸發側重於溶劑離開留溶質,蒸餾則靠沸點差分離揮發性組分。