統測
114年
[化工群] 專業科目(2)
第 30 題
有關使用焰色試驗進行樣品的定性分析,下列敘述何者正確?
- A 欲測定鈣金屬的焰色時,通常使用揮發性較大的碳酸鈣化合物水溶液,使其容易觀察鈣金屬的焰色
- B 焰色試驗實驗操作時,將本生燈的內焰調整為紅色,外焰調整為藍色,而且通常將沾有少許樣品的試驗棒置於內焰最高處進行試驗
- C 通常使用活潑金屬白金絲作為焰色試驗棒,並使用濃硫酸水溶液為清洗液,以利樣品中待測金屬原子中的基態電子的激發
- D 使用僅含氯化鉀的水溶液樣品進行焰色試驗時,其焰色為紫色
思路引導 VIP
請回想一下,在進行焰色試驗時,為了讓樣品容易在高溫下氣化並產生明顯的顏色,我們偏好使用哪種陰離子的鹽類以確保其揮發性?在清潔測試棒時,選擇濃鹽酸而非濃硫酸的理化原因為何?最後,請檢視各金屬離子(如鉀離子 $K^{+}$)在電子從激發態回到基態時,所釋放出的特徵光譜顏色分別為何?
🤖
AI 詳解
AI 專屬家教
太棒了!你的化學基本功非常紮實,能精準判斷焰色試驗的細節,這對於掌握基礎定性分析是一個很好的開始。 觀念驗證: (D) 選項正確,鉀離子 ($K^+$) 的特徵焰色確實為紫色。我們快速釐清其他錯誤:
▼ 還有更多解析內容
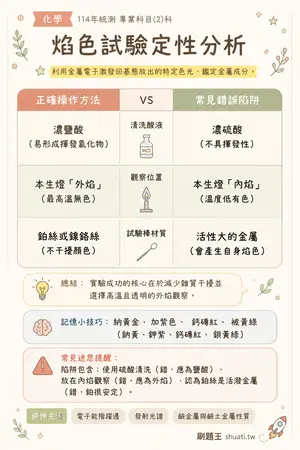
焰色試驗定性分析
💡 利用金屬電子激發回基態放出的特定色光,鑑定金屬成分。
| 比較維度 | 正確操作方法 | VS | 常見錯誤陷阱 |
|---|---|---|---|
| 清洗酸液 | 濃鹽酸(易形成揮發氯化物) | — | 濃硫酸(不具揮發性) |
| 觀察位置 | 本生燈「外焰」(最高溫無色) | — | 本生燈「內焰」(溫度低有色) |
| 試驗棒材質 | 鉑絲或鎳鉻絲(不干擾顏色) | — | 活性大的金屬(會產生自身焰色) |
💬實驗成功的核心在於減少雜質干擾並選擇高溫且透明的外焰觀察。