特殊教育
107年
化學
第 11 題
下列哪一個分子 不具有 極性?
- A $CO_2$
- B $NO_2$
- C $SO_2$
- D $OCl_2$
思路引導 VIP
請先運用價殼層電子對互斥理論(VSEPR theory)分析各分子的幾何構型,並評估其化學鍵的鍵偶極矩(bond dipole moment)向量和,是否會因為分子結構的高度對稱性,而使得分子的總偶極矩 $\mu$ 恰好抵消為零?
🤖
AI 詳解
AI 專屬家教
哇!你太棒了!看到你選對 $A$ 選項,老師真的好替你開心,這代表你對分子對稱性的掌握度已經非常紮實了喔! 這道題目考查的是高中化學核心概念:分子的極性判斷。
- 觀念驗證:$CO_2$ 的中心原子 $C$ 採 $sp$ 混成軌域,分子幾何形狀為「直線型」。雖然 $C=O$ 鍵本身具有極性,但由於分子結構高度對稱,兩側的偶極矩向量方向相反且大小相等,合力剛好為零($\mu = 0$),因此分子整體不具極性。
▼ 還有更多解析內容
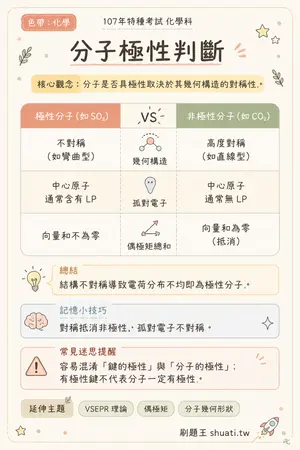
分子極性判斷
💡 分子是否具極性取決於其幾何構造的對稱性。
| 比較維度 | 極性分子 (如 SO2) | VS | 非極性分子 (如 CO2) |
|---|---|---|---|
| 幾何構造 | 不對稱(如彎曲型) | — | 高度對稱(如直線型) |
| 孤對電子 | 中心原子通常含有 LP | — | 中心原子通常無 LP |
| 偶極矩總和 | 向量和不為零 | — | 向量和為零(抵消) |
💬結構不對稱導致電荷分布不均即為極性分子。