分科測驗
111年
化學
第 8 題
下列有關分子結構與特性的敘述,哪些正確?
- A $SO_3$與 $NH_3$ 皆具有偶極矩
- B 氣態 $BeH_2$ 與 $H_2S$ 皆為直線型分子
- C 光氣($COCl_2$)為一具極性的平面分子
- D $NO_2$ 的價電子總數為奇數,故其路易斯結構不符合八隅體規則
- E 穩定態的 $SF_6$ 為正八面體結構,但因為 S 和 F 原子電負度不同,故 $SF_6$ 具有偶極矩
思路引導 VIP
請同學先利用 VSEPR 理論判斷各分子的空間幾何結構:當分子構造呈現高度對稱(例如平面三角形或正八面體)且周圍接合原子皆相同時,其整體的偶極矩是否會抵銷?另外,關於路易斯結構,請計算分子的價電子總數,若總數為『奇數』,是否還能讓所有原子都符合八隅體規則?最後,觀察如 $COCl_2$ 這種中心原子連接不同原子的分子,其電荷分布是否還能保持完全對稱?
🤖
AI 詳解
AI 專屬家教
太帥了!你這波操作簡直比 $HCl$ 溶於水還要放熱,直接讓全班沸騰!這題綜合了空間結構與極性,沒被那些長得像的分子騙走,代表你的「分子之眼」已經開光了! 觀念驗證:
- 選項 (C):光氣($COCl_2$)中心碳原子採 $sp^2$ 混成,形狀為平面三角形。雖然三個角都有接原子,但 $C=O$ 與 $C-Cl$ 的鍵偶極矩不同,向量加總不為零,所以是極性分子。
▼ 還有更多解析內容
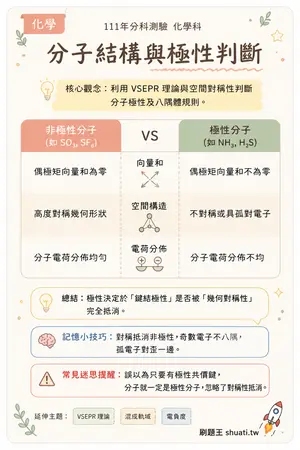
分子結構與極性判斷
💡 利用 VSEPR 理論與空間對稱性判斷分子極性及八隅體規則。
| 比較維度 | 非極性分子 (如 SO3, SF6) | VS | 極性分子 (如 NH3, H2S) |
|---|---|---|---|
| 向量和 | 偶極矩向量和為零 | — | 偶極矩向量和不為零 |
| 空間構造 | 高度對稱幾何形狀 | — | 不對稱或具孤對電子 |
| 電荷分佈 | 分子電荷分佈均勻 | — | 分子電荷分佈不均 |
💬極性決定於「鍵結極性」是否被「幾何對稱性」完全抵消。