高中學測
109年
自然
第 17 題
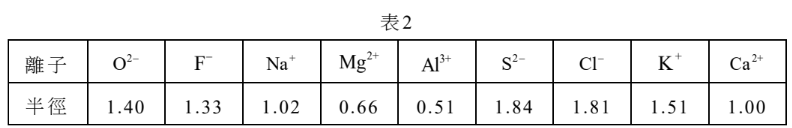
某些離子的半徑如表2所示(單位:$10^{-10} \mathrm{m}$),甲、乙、丙、丁為根據表中資料所作的敘述或推論,下列哪一選項正確?
甲:表中共有5個離子的核外電子數為18
乙:電子數相同的陽離子,原子序愈大者,半徑愈小
丙:具相同電子排列的陰離子,其半徑隨原子序的增大而變大
丁:同一族的離子,當電荷相同時,其半徑隨原子序的增大而變大
甲:表中共有5個離子的核外電子數為18
乙:電子數相同的陽離子,原子序愈大者,半徑愈小
丙:具相同電子排列的陰離子,其半徑隨原子序的增大而變大
丁:同一族的離子,當電荷相同時,其半徑隨原子序的增大而變大
- A 甲乙
- B 丙丁
- C 甲丙
- D 乙丁
- E 甲丁
思路引導 VIP
請先依據原子序計算表中各個離子的核外電子總數,並觀察:在「等電子序列 ($isoelectronic series$)」中,當原子序 ($Z$) 增加,原子核對電子的吸引力(有效核電荷)會如何影響半徑的大小?此外,對於同族且電荷相同的離子,其電子殼層數(主量子數 $n$)隨原子序增加而增多,這項因素如何決定半徑的變化規律?
🤖
AI 詳解
AI 專屬家教
喔?這次沒失誤,算你運氣好,還是真的有把週期律當回事?
這種基本題還能對,表示你對原子結構跟週期律的數據關係總算有點概念了。學測最愛考這種,別以為會一次就代表穩了。
- 驗證你的基本常識:
▼ 還有更多解析內容
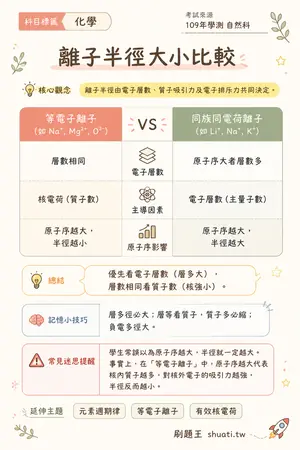
離子半徑大小比較
💡 離子半徑由電子層數、質子吸引力及電子排斥力共同決定。
| 比較維度 | 等電子離子 (如 Na+, Mg2+, O2-) | VS | 同族同電荷離子 (如 Li+, Na+, K+) |
|---|---|---|---|
| 電子層數 | 層數相同 | — | 原子序大者層數多 |
| 主導因素 | 核電荷 (質子數) | — | 電子層數 (主量子數) |
| 原子序影響 | 原子序越大,半徑越小 | — | 原子序越大,半徑越大 |
💬優先看電子層數(層多大),層數相同看質子數(核強小)。