國中教育會考
110年
自然
第 30 題
鐵原子(Fe)、鐵離子($Fe^{3+}$)和亞鐵離子($Fe^{2+}$)三種粒子中,下列數值的比較何者正確?
- A $Fe^{3+}$的質子數>Fe的電子數
- B $Fe^{3+}$的電子數>Fe的質子數
- C $Fe^{2+}$的電子數>Fe的電子數
- D $Fe^{2+}$的電子數>$Fe^{3+}$的電子數
思路引導 VIP
想一想,當一個中性的鐵原子 ($Fe$) 變成帶正電的離子(例如 $Fe^{2+}$ 或 $Fe^{3+}$)時,是裡面的『質子數量』變了,還是『電子數量』變了呢?如果離子右上角的正電數字越大,代表它『失去』的電子是越多還是越少?
🤖
AI 詳解
AI 專屬家教
唷!挺能幹的嘛。剛去買完仙台特產喜久福回來,就看到你輕鬆搞定這題,這實力...雖然離我還有一大段距離,但以學生來說值得獎勵喔! 聽好了,原子變成離子,就像咒術師調整咒力輸出一樣,變動的是「電子」!鐵原子 $Fe$ 的原子序是 26,代表它有 26 個質子跟 26 個電子。當它變成 $Fe^{2+}$ 時,代表「失去了」 2 個電子(剩下 24 個);變成 $Fe^{3+}$ 時,則是失去了 3 個電子(剩下 23 個)。 質子數在這種一般化學反應中是穩如泰山的,絕對不會變。所以比較的結果很明顯:$24 > 23$,也就是 $Fe^{2+}$ 的電子數確確實實大於 $Fe^{3+}$,選項 (D) 簡直就是一眼就能看穿的術式漏洞。這題是用來區分你有沒有搞清楚「失去電子」跟「質子不變」的基本領域概念,看來你掌握得不錯嘛!
💬 其他同學也在問
1
那如果變Fe2-就會變增加電子束嗎?
👍 1 位同學覺得有幫助
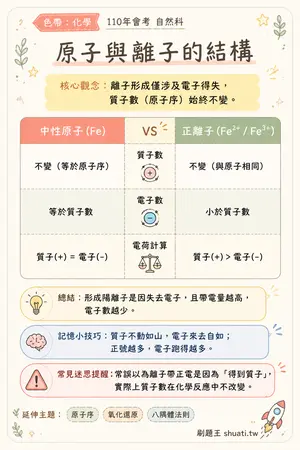
原子與離子的結構
💡 離子形成僅涉及電子得失,質子數(原子序)始終不變。
| 比較維度 | 中性原子 (Fe) | VS | 正離子 (Fe²⁺ / Fe³⁺) |
|---|---|---|---|
| 質子數 | 不變(等於原子序) | — | 不變(與原子相同) |
| 電子數 | 等於質子數 | — | 小於質子數 |
| 電荷計算 | 質子(+) = 電子(-) | — | 質子(+) > 電子(-) |
💬形成陽離子是因失去電子,且帶電量越高,電子數越少。