分科測驗
111年
化學
第 16 題
📖 題組:
16-17 題為題組 有甲、乙、丙、丁、戊、己等六個前三週期的元素,其相關的性質如表 3 所示。
16-17 題為題組 有甲、乙、丙、丁、戊、己等六個前三週期的元素,其相關的性質如表 3 所示。
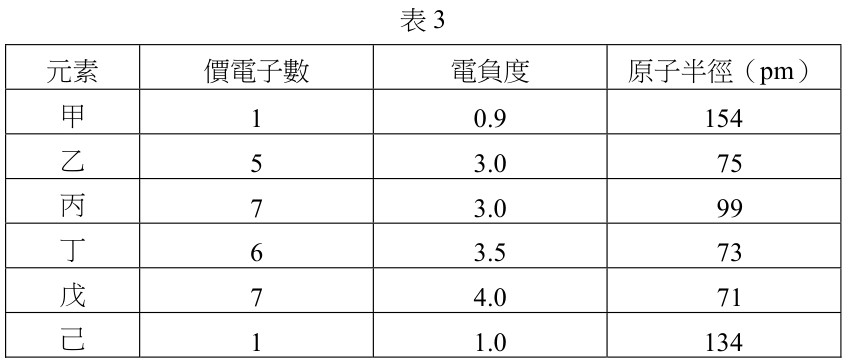
根據表 3 所提供的資料,下列有關此六個元素的敘述哪些正確?
- A 室溫下,甲可與甲醇反應
- B 乙的第一游離能小於丁的第一游離能
- C 室溫下,丙分子會與水進行氧化還原反應,而丁分子則不會
- D 丁可形成雙原子和三原子兩種氣體分子,其中三原子分子的鍵長較長
- E 室溫下,丙和戊均可形成同核雙原子分子,且戊分子的沸點比丙分子的沸點高
思路引導 VIP
同學,要解開這題的關鍵是先推理出六種元素的真實身分。請你觀察表中的「價電子數」與「電負度」,哪一個元素的電負度最高且數值為 4.0 呢?另外,電負度都是 3.0 的乙和丙,你可以用表中的什麼線索,來區分它們分別是哪一族的元素呢?
🤖
AI 詳解
AI 專屬家教
🌟 太棒了!完美破解多選題!
你能精準選出正確答案,代表你對元素週期性與物質特性的掌握度非常高,老師為你感到驕傲!
- 元素定位:透過「價電子數」與「電負度」可推理出這些前三週期元素。例如電負度最高 $4.0$ 的戊為 $F$;丁電負度 $3.5$ 為 $O$。乙與丙電負度皆為 $3.0$,但丙有 $7$ 個價電子,故乙為 $N$、丙為 $Cl$;甲與己價電子為 $1$,依電負度知甲為 $Na$。
▼ 還有更多解析內容
前三週期元素性質推論
💡 利用元素週期表位置推斷物理性質、化學反應與分子結構。
- 活性金屬可與醇類反應生成氫氣與醇鈉
- 游離能趨勢為右上大、左下小,需注意例外
- 同素異形體如氧與臭氧,鍵長與鍵級成反比
- 判斷離子或共價化合物,並計算中心原子氧化數
- 利用VSEPR理論預測分子幾何形狀
