分科測驗
112年
化學
第 19 題
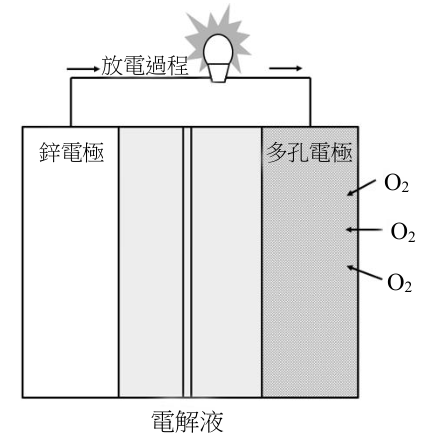
二次電池與我們的日常生活息息相關,鋰離子電池便是一例。近年來科學家開始發展一種同時具備金屬離子電池與燃料電池優點的二次電池,以鋅-空氣電池(圖4)為例,放電時電極反應如式3和式4所示:
$Zn + 2OH^- \rightarrow ZnO + H_2O + 2e^-$ (式3)
$O_2 + 4H^+ + 4e^- \rightarrow 2H_2O$ (式4)
下列關於鋅-空氣電池的敘述,哪些正確?
$Zn + 2OH^- \rightarrow ZnO + H_2O + 2e^-$ (式3)
$O_2 + 4H^+ + 4e^- \rightarrow 2H_2O$ (式4)
下列關於鋅-空氣電池的敘述,哪些正確?
- A 在放電過程中,金屬鋅為陰極
- B 在放電過程中,陰極的產物為水
- C 此電池的全反應為 $2Zn + O_2 \rightarrow 2ZnO$
- D 若將此電池的金屬鋅換成鎂,則無法進行放電反應
- E 若需對此電池進行充電,在充電過程中,水會氧化產生氧氣
思路引導 VIP
在遇到這類提供半反應式的電池題目時,你會如何透過觀察「電子的得失」來找出哪一極是陽極、哪一極是陰極?接著,如果要推導「充電」時的反應,你會如何利用剛才找出的放電反應來進行反向推理呢?
鋅空氣電池原理
💡 掌握電池放電與充電時的氧化還原反應與電極性質。
- 放電時負極(陽極)發生氧化,正極(陰極)發生還原
- 全反應式為兩半反應相加,並將電子項消去後的結果
- 充電為放電的逆反應,原本的產物會被氧化或還原
- 電子由負極經外電路流向正極,正極產物依反應式判定
