分科測驗
110年
化學
第 10 題
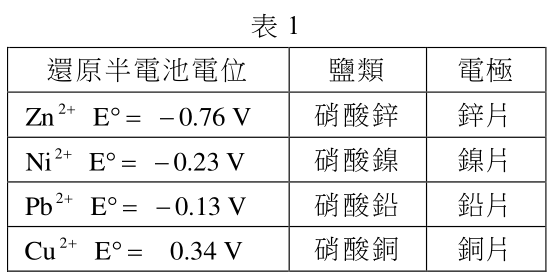
王同學欲進行化學電池實驗,查出 4 種半電池標準還原電位,如表 1 所示,並取得相關的純水、鹽橋、燒杯、鹽類及電極。王同學取出兩種半電池,並以鹽橋連結組合後,構成化學電池,如圖 3 所示。
下列實驗條件及其結果的敘述,何者正確?
下列實驗條件及其結果的敘述,何者正確?
- A 測得電壓為 0.57 V 的電池中,銅片為正極
- B 鎳鋅電池中,鎳片為陽極
- C 鎳鉛電池所測得電壓會大於 0.36 V
- D 將鹽橋移除改用銅線,仍可組成電池
- E 將半電池的金屬換成石墨,仍可組成電池
思路引導 VIP
如果你要在實驗室裡,利用表格中的半電池搭配出一個產生特定電壓的電池,你會如何使用這些『還原半電池電位』的數據來列式計算呢?另外,在決定好兩種金屬組合後,你又是根據什麼原則來判斷哪一端該接在電池的正極?
化學電池與電位計算
💡 利用標準還原電位差計算電動勢,並辨別正負極。
- 電位高者為正極(陰極),電位低者為負極(陽極)。
- 全電池電位 = 正極還原電位 - 負極還原電位。
- 鹽橋維持電中性及溝通電路,不可用一般導線代替。
- 負極(陽極)發生氧化,正極(陰極)發生還原。
