分科測驗
111年
化學
第 3 題
📖 題組:
3-4 題為題組 實驗課時進行電解濃食鹽水的實驗,實驗設計是以碳棒做為電極。大部分的學生實驗結果如圖 2 所示,陰極與陽極皆會產生氣體,且甲管與乙管的液面高度大致相同。 (圖2及表1) 但是,有五組的學生誤將其他鹽類當成食鹽配成水溶液進行電解實驗。誤拿的五種鹽類,事後發現應為亞硫酸鈉、硝酸銀、氯化鉀、硫酸鎂、硝酸鈉。學生找資料查到可能相關的標準還原電位數據,如表 1 所示。
3-4 題為題組 實驗課時進行電解濃食鹽水的實驗,實驗設計是以碳棒做為電極。大部分的學生實驗結果如圖 2 所示,陰極與陽極皆會產生氣體,且甲管與乙管的液面高度大致相同。 (圖2及表1) 但是,有五組的學生誤將其他鹽類當成食鹽配成水溶液進行電解實驗。誤拿的五種鹽類,事後發現應為亞硫酸鈉、硝酸銀、氯化鉀、硫酸鎂、硝酸鈉。學生找資料查到可能相關的標準還原電位數據,如表 1 所示。
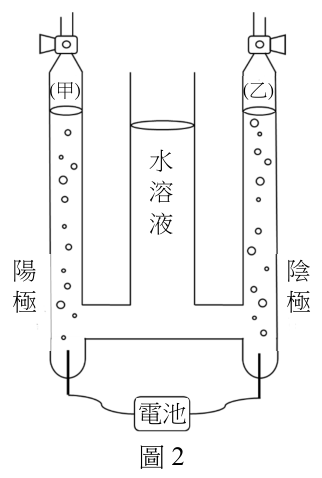

在大部分學生正確使用濃食鹽水的結果中,甲管的氣體應為下列何者?
- A 氫氣
- B 氧氣
- C 氮氣
- D 氯氣
- E 二氧化氮
思路引導 VIP
我們一步步來破解這題:請先觀察圖 2,甲管所在的一端是標示「陽極」還是「陰極」?這代表它應該發生「氧化」還是「還原」反應呢?確認之後,請你想想看,在濃食鹽水裡面,有哪些物質跑到該電極時,可能會參與這個反應?
🤖
AI 詳解
AI 專屬家教
1. 大力肯定
太棒了!你非常精準地選出了正確答案!這題考查了電解水溶液的核心觀念,你能注意到題目中「濃」食鹽水這個關鍵字,代表你的電化學底子非常扎實,思考十分嚴謹!
2. 觀念驗證
▼ 還有更多解析內容
電解水溶液產物判斷
💡 依還原電位判斷競爭反應,確認陰陽兩極的產物與狀態。
- 陰極優先還原電位大者,活性大金屬離子不反應。
- 陽極優先氧化電位大者,亞硫酸根與鹵離子易反應。
- 銀離子還原成銀、亞硫酸根氧化成硫酸根,均不產氣。
- 濃食鹽水陽極生氯氣,陰極生氫氣,體積比約一比一。
