高中學測
113年
自然
第 13 題
📖 題組:
黃鐵礦($FeS_2$)是地表上主要礦物之一,通常與他種岩石的硫化物或氧化物伴生。地質學家為了了解黃鐵礦成分,進行以下的實驗。其實驗步驟如下: 步驟1:將黃鐵礦實驗樣品磨成粉末,於3個錐形瓶(標號1~3)中分別放置0.35克樣品,並加入50 mL的酸性溶液。 步驟2:將3個錐形瓶置放在室溫,但不同氧氣分壓下。 步驟3:經過一天後,取出20 mL上層澄清液,測量溶液中含鐵總濃度($[Fe_{total}]$,包含Fe(II)與Fe(III))、$SO_4^{2-}$濃度($[SO_4^{2-}]$)及含硫總濃度($[S_{total}]$,包含$[SO_4^{2-}]$與其它含硫物質濃度)。 上述含硫總濃度是先用化學方法,將溶液中所有硫化物氧化成$SO_4^{2-}$後,再加以測量,實驗結果列於表1。
黃鐵礦($FeS_2$)是地表上主要礦物之一,通常與他種岩石的硫化物或氧化物伴生。地質學家為了了解黃鐵礦成分,進行以下的實驗。其實驗步驟如下: 步驟1:將黃鐵礦實驗樣品磨成粉末,於3個錐形瓶(標號1~3)中分別放置0.35克樣品,並加入50 mL的酸性溶液。 步驟2:將3個錐形瓶置放在室溫,但不同氧氣分壓下。 步驟3:經過一天後,取出20 mL上層澄清液,測量溶液中含鐵總濃度($[Fe_{total}]$,包含Fe(II)與Fe(III))、$SO_4^{2-}$濃度($[SO_4^{2-}]$)及含硫總濃度($[S_{total}]$,包含$[SO_4^{2-}]$與其它含硫物質濃度)。 上述含硫總濃度是先用化學方法,將溶液中所有硫化物氧化成$SO_4^{2-}$後,再加以測量,實驗結果列於表1。
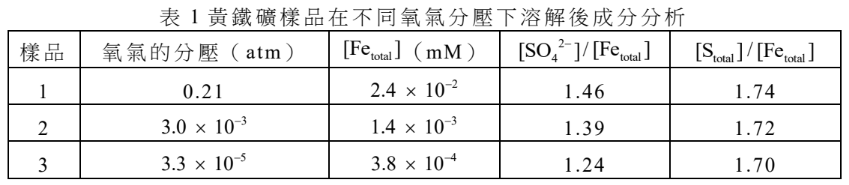
下列實驗觀察哪些為合理敘述?(應選3項)
- A 理論上純度100%的黃鐵礦樣品,其 $[S_{total}] / [Fe_{total}]$ 值應該為2
- B 黃鐵礦在酸性溶液中,會隨氧氣分壓增高而減少其溶解的量
- C 此實驗黃鐵礦樣品中可能含有氧化鐵,所以量測 $[S_{total}] / [Fe_{total}]$ 的值小於2
- D 在純氮氣下操作此實驗,$[SO_4^{2-}] / [Fe_{total}]$ 的值會大於1.46
- E 表1中,$[SO_4^{2-}] / [Fe_{total}]$ 值比 $[S_{total}] / [Fe_{total}]$ 值小,表示在氧氣分壓為0.21 atm,經過一天仍無法將硫化物都氧化成 $SO_4^{2-}$
思路引導 VIP
請同學先觀察黃鐵礦的化學式 $FeS_2$,其理論上的硫鐵原子數比與實驗觀測到的 $\frac{[S_{total}]}{[Fe_{total}]}$ 有何差異?這種差異可能暗示樣品中含有什麼不含硫的雜質?接著,請分析表 1 中隨著氧氣分壓的增加,$[Fe_{total}]$ 的濃度變化趨勢,以及 $\frac{[SO_4^{2-}]}{[Fe_{total}]}$ 與 $\frac{[S_{total}]}{[Fe_{total}]}$ 兩者之間的差距,這對於判斷溶解量以及硫原子的氧化程度有何物理化學意義?
🤖
AI 詳解
AI 專屬家教
同學,看來你被「氮氣」給邊緣化了喔!雖然你精準抓到了 $FeS_2$ 的基本計量 (A) 與雜質對比例的影響 (C),但在數據趨勢面前,你居然被 (D) 唬住了。 【迷思破解】 你選 (D) 表示你覺得沒氧氣反應反而更強?看表 1 數據,氧氣分壓從 $0.21 \text{ atm}$ 降到 $3.3 \times 10^{-5} \text{ atm}$ 時,$[SO_4^{2-}] / [Fe_{total}]$ 的值從 $1.46$ 一路下滑到 $1.24$。這說明氧氣是反應物,氧氣越少,硫被氧化成硫酸根的比例就越低。純氮氣(無氧)下,這比例只會探底,絕不可能大於 $1.46$!
▼ 還有更多解析內容