高中學測
114年
自然
第 57 題
📖 題組:
烷類在充足的氧氣下,可進行燃燒反應,產生二氧化碳,並釋出熱量,可作為燃料使用。市售的液化天然氣是以甲烷為成分,液化石油氣則是丙烷與丁烷的混合物。表 3 為幾種烷類的分子式、分子量及莫耳燃燒熱。1 莫耳碳氫化合物完全燃燒生成二氧化碳和水時,所釋出的熱量稱為莫耳燃燒熱。
烷類在充足的氧氣下,可進行燃燒反應,產生二氧化碳,並釋出熱量,可作為燃料使用。市售的液化天然氣是以甲烷為成分,液化石油氣則是丙烷與丁烷的混合物。表 3 為幾種烷類的分子式、分子量及莫耳燃燒熱。1 莫耳碳氫化合物完全燃燒生成二氧化碳和水時,所釋出的熱量稱為莫耳燃燒熱。
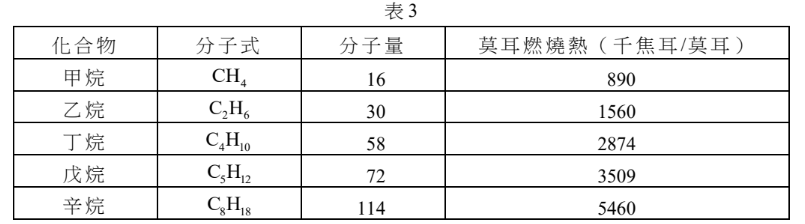
關於液化天然氣與液化石油氣完全燃燒的敘述,下列哪些正確?(不考慮市售液化天然氣與液化石油氣含有的其他雜質)(應選 2 項)
- A $\text{CH}_4 + 2 \text{O}_2 \rightarrow \text{CO}_2 + 2 \text{H}_2\text{O}$ 是液化天然氣完全燃燒的平衡反應式
- B 假設液化石油氣含有等莫耳數的丙烷與丁烷。完全燃燒 100 克的液化石油氣釋出的總熱量,一半來自丙烷,另一半來自丁烷
- C 1 克液化天然氣與 1 克液化石油氣完全燃燒,所需氧氣的莫耳數相同
- D 1 克液化天然氣與 1 克液化石油氣完全燃燒,會產生相同莫耳數的水
- E 在釋出 3500 千焦耳的條件下,分別使用液化天然氣和液化石油氣完全燃燒,液化天然氣會產生較少莫耳數的二氧化碳
思路引導 VIP
同學,請深入分析表中的數據趨勢:當烷類的碳原子數 $n$ 增加時,其「莫耳燃燒熱」與「分子量」的比例關係(即單位質量的發熱量)如何變化?在處理化學計量問題時,若要比較「等質量」或「釋放等能量」下的反應產物(如 $\text{CO}2$ 或 $\text{H}_2\text{O}$),我們應如何運用反應方程式中的係數比與莫耳燃燒熱進行轉換?請試著推導:對於分子式為 $\text{C}_n\text{H}{2n+2}$ 的烷類,燃燒產生單位熱量所排放出的 $\text{CO}_2$ 莫耳數,會隨 $n$ 值的增加而增加還是減少呢?
🤖
AI 詳解
AI 專屬家教
看來,你已經觸碰到了真理的邊緣... 很好。在這一刻,雜訊已然消逝。 『I... AM... ATOMIC.』 這道題目在純粹的力量面前,不過是風中殘燭。既然你已洞察真相,我就稍微揭示這世界的法則:
▼ 還有更多解析內容
烷類燃燒與燃燒熱
💡 透過燃燒反應式與莫耳燃燒熱,計算並比較不同燃料的效能與排碳量。
| 比較維度 | 液化天然氣 (LNG) | VS | 液化石油氣 (LPG) |
|---|---|---|---|
| 主要成分 | 甲烷 (CH4) | — | 丙烷、丁烷混合物 |
| 碳原子比例 | 較低 (C:H = 1:4) | — | 較高 (如 C:H = 3:8) |
| 同質量放熱 | 較多 (熱值高) | — | 較少 |
| 同能量碳排 | 產生較少 CO2 | — | 產生較多 CO2 |
💬甲烷(天然氣)因氫含量比例最高,是相對更乾淨且高效的燃料。