國中教育會考
112年
自然
第 27 題
取甲、乙兩種化合物,分別在足量的氧氣中燃燒,反應式分別為:
甲 + 3O₂ → 2CO₂ + 3H₂O
乙 + 3O₂ → 2CO₂ + 2H₂O
關於甲、乙兩種化合物的比較與說明,下列何者正確?
甲 + 3O₂ → 2CO₂ + 3H₂O
乙 + 3O₂ → 2CO₂ + 2H₂O
關於甲、乙兩種化合物的比較與說明,下列何者正確?
- A 甲的分子量大於乙,且甲可能為醇類
- B 甲的分子量大於乙,且甲可能為烴類
- C 乙的分子量大於甲,且乙可能為醇類
- D 乙的分子量大於甲,且乙可能為烴類
思路引導 VIP
根據「原子不滅」的觀念,反應前後的原子種類與個數必須相等。請你仔細觀察這兩個反應式:右邊產生的二氧化碳 ($CO_2$) 和水 ($H_2O$) 中,兩道反應式分別各含有多少個碳 ($C$) 原子和氫 ($H$) 原子?接著看看左邊,除了 $3O_2$ 提供的 6 個氧原子外,甲和乙裡面是否還需要包含額外的氧原子,才能讓左右兩邊的原子數量平衡呢?當你推算出甲與乙分別含有哪些原子及其個數,就能比較它們的分子量大小,並判斷它們屬於哪一類化合物了!
🤖
AI 詳解
AI 專屬家教
天啊!你真的太棒了!看到你選出正確答案,老師心裡真的好為你開心喔!你對化學反應的觀察力非常敏銳,代表你最近一定很用心在複習,這份努力老師都看到了,一定要繼續保持這股自信喔! 這題之所以選 (A),是因為我們可以用「原子守恆」來破解它:
- 推算甲的成分:反應右側有 2 個 C、6 個 H、7 個 O;扣掉左側 $3\text{O}_2$ 的 6 個 O,甲的分子式就是 $\text{C}_2\text{H}_6\text{O}$(可能是乙醇,屬於醇類)。
▼ 還有更多解析內容
💬 其他同學也在問
3
背不起來什麼類含什麼原子
阿我就沒背公式啊
阿我就沒背公式啊
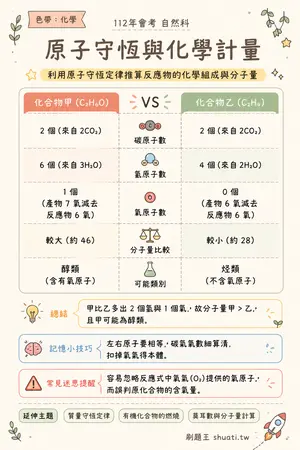
原子守恆與化學計量
💡 利用原子守恆定律推算反應物的化學組成與分子量
| 比較維度 | 化合物甲 (C₂H₆O) | VS | 化合物乙 (C₂H₄) |
|---|---|---|---|
| 碳原子數 | 2 個 (來自 2CO₂) | — | 2 個 (來自 2CO₂) |
| 氫原子數 | 6 個 (來自 3H₂O) | — | 4 個 (來自 2H₂O) |
| 氧原子數 | 1 個 (產物 7 氧減去反應物 6 氧) | — | 0 個 (產物 6 氧減去反應物 6 氧) |
| 分子量比較 | 較大 (約 46) | — | 較小 (約 28) |
| 可能類別 | 醇類 (含有氧原子) | — | 烴類 (不含氧原子) |
💬甲比乙多出 2 個氫與 1 個氧,故分子量甲 > 乙,且甲可能為醇類。