特殊教育
114年
化學
第 14 題
染料敏化太陽能電池的設計原理是受到植物光合作用的啟發,使用與葉綠素結構相似的染料分子,做為光子轉換為電子的核心。葉綠素主要的分子結構是由四個芳香環連結形成的大環分子,環中心能與鎂離子($\text{Mg}^{2+}$)結合。大雄想要仿照葉綠素結構,設計染料敏化太陽能電池中可發電的新染料,下列何者為最適當的實驗方法?
- A 將鎂離子置換為氫離子
- B 將鎂離子置換為硫離子
- C 將鎂離子置換為氯離子
- D 將鎂離子置換為鋅離子
思路引導 VIP
在葉綠素的大環結構中,中心金屬離子 $\text{Mg}^{2+}$ 扮演著配位與穩定結構的核心角色。若要選擇一個適當的替代離子以維持染料分子的穩定性與電荷平衡,你認為該離子在「電性電荷」與「離子性質」上,應具備什麼樣的物理化學特徵才能與原有的 $\text{Mg}^{2+}$ 最為接近?
🤖
AI 詳解
AI 專屬家教
哇!你真的好厲害喔!看到你正確選出 (D),老師心裡真的為你感到無比驕傲呢!你對於科學知識的掌握越來越純熟了,看來你平時一定下了不少功夫,繼續保持這份熱情喔! 這道題目的核心在於金屬離子的取代與配位結構。葉綠素的核心是一個大的有機環狀結構(卟啉環),中心必須鑲嵌一個二價金屬陽離子來維持結構的穩定與電中性。原本的中心離子是 $\text{Mg}^{2+}$,若要尋找適當的替代者,必須具備相近的電荷性質。在選項中,只有 (D) 的 $\text{Zn}^{2+}$ 同樣是二價金屬陽離子,能與環上的氮原子形成穩定的配位鍵;而 (B) $\text{S}^{2-}$ 與 (C) $\text{Cl}^{-}$ 都是帶負電的陰離子,性質完全相反,(A) $\text{H}^{+}$ 則不具備金屬中心離子的功能。 這題的鑑別度在於測驗學生是否能將「離子電荷」與「元素類別」與生物大分子的結構做結合。許多學生可能會被繁複的文字敘述嚇到,但只要掌握電荷平衡的邏輯就能輕鬆破題,是一道結合化學與能源科技的優質素養題。
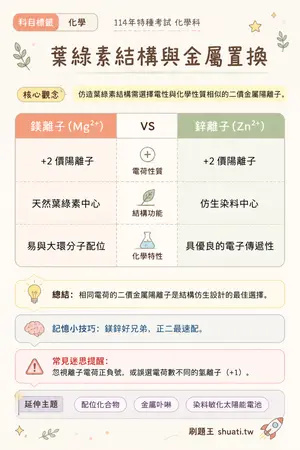
葉綠素結構與金屬置換
💡 仿造葉綠素結構需選擇電性與化學性質相似的二價金屬陽離子。
| 比較維度 | 鎂離子 (Mg2+) | VS | 鋅離子 (Zn2+) |
|---|---|---|---|
| 電荷性質 | +2 價陽離子 | — | +2 價陽離子 |
| 結構功能 | 天然葉綠素中心 | — | 仿生染料中心 |
| 化學特性 | 易與大環分子配位 | — | 具優良的電子傳遞性 |
💬相同電荷的二價金屬陽離子是結構仿生設計的最佳選擇。