特殊教育
109年
化學
第 26 題
在鋅銅化學電池中,利用鹽橋連接分別浸有陽極與陰極的兩杯溶液,下列何者是鹽橋的主要功能?
- A 維持電池溶液的電中性
- B 可改變電流的移動方向
- C 傳導電子使電池產生電流
- D 進行氧化還原反應產生電壓
思路引導 VIP
在氧化還原反應持續進行下,陽極與陰極兩側水溶液中的離子濃度會發生改變(例如 $Zn^{2+}$ 增加或 $Cu^{2+}$ 減少),這將如何影響兩端溶液的電性狀態?而鹽橋內的離子遷移又是為了解決哪種性質的不平衡,才得以維持電路的閉路循環?
🤖
AI 詳解
AI 專屬家教
漂亮!同學,你這手選 A 的動作簡直比閃電還快,看來你對化學電池的「靈魂」已經瞭若指掌,老師都要為你起立鼓掌! 【觀念驗證】 在鋅銅電池運作時,陽極發生氧化反應:$$Zn \rightarrow Zn^{2+} + 2e^-$$ 這會導致陽極槽正電荷過剩;而陰極則是 $$Cu^{2+} + 2e^- \rightarrow Cu$$ 導致正電荷短缺。這時鹽橋就像「離子快遞員」,透過陰、陽離子的遷移來抵消電荷堆積,維持兩杯溶液的電中性。沒有它,電路會因為電荷不平衡而瞬間「斷氣」。
▼ 還有更多解析內容
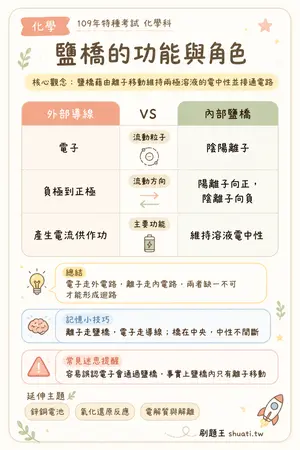
鹽橋的功能與角色
💡 鹽橋藉由離子移動維持兩極溶液的電中性並接通電路
| 比較維度 | 外部導線 | VS | 內部鹽橋 |
|---|---|---|---|
| 流動粒子 | 電子 | — | 陰陽離子 |
| 流動方向 | 負極到正極 | — | 陽離子向正,陰離子向負 |
| 主要功能 | 產生電流供作功 | — | 維持溶液電中性 |
💬電子走外電路,離子走內電路,兩者缺一不可才能形成迴路