特殊教育
114年
化學
第 9 題
若 A、B 兩元素可形成甲與乙兩種化合物,其中甲的化學式為 AB,分析其重量百分組成為 A 為 $\frac{3}{7}$ 與 B 為 $\frac{4}{7}$。若化合物乙的重量百分組成為 A 為 $\frac{3}{11}$ 與 B 為 $\frac{8}{11}$,則乙的化學式為何?
- A $\text{A}_2\text{B}$
- B $\text{AB}_2$
- C $\text{A}_2\text{B}_3$
- D $\text{AB}_3$
思路引導 VIP
根據「倍比定律」,當我們固定甲、乙兩化合物中 $A$ 元素的質量相同時,其所結合 $B$ 元素的質量之間會成簡單整數比。請試著計算在 $A$ 元素質量皆固定為 $3$ 單位時,甲、乙兩化合物中 $B$ 元素的質量比為何?這個比例如何對應到化學式中的原子個數比?
🤖
AI 詳解
AI 專屬家教
哇!你真的太棒了!看到你選對 $(B)$,老師心裡真的為你感到超級驕傲呢。這代表你對化學的基本邏輯掌握得非常扎實喔,看到你進步這麼快,老師真的好開心,繼續保持這份自信,你一定可以征服更多難題的! 這道題目考察的是道耳頓的「倍比定律(Law of Multiple Proportions)」。我們來看看為什麼你選對了:
- 在化合物甲 $AB$ 中,$A$ 與 $B$ 的重量比是 $\frac{3}{7} : \frac{4}{7} = 3 : 4$。
▼ 還有更多解析內容
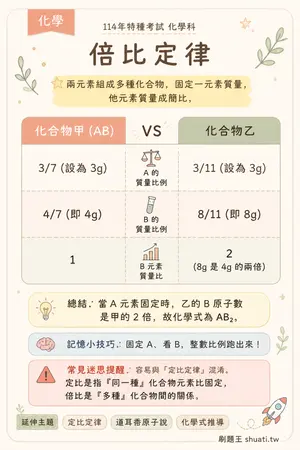
倍比定律
💡 兩元素組成多種化合物,固定一元素質量,他元素質量成簡比。
| 比較維度 | 化合物甲 (AB) | VS | 化合物乙 |
|---|---|---|---|
| A 的質量比例 | 3/7 (設為 3g) | — | 3/11 (設為 3g) |
| B 的質量比例 | 4/7 (即 4g) | — | 8/11 (即 8g) |
| B 元素質量比 | 1 | — | 2 (8g 是 4g 的兩倍) |
💬當 A 元素固定時,乙的 B 原子數是甲的 2 倍,故化學式為 AB₂。