統測
114年
[化工群] 專業科目(2)
第 8 題
在學習了原子結構與週期表的單元後,甲、乙、丙、丁、戊五位同學分別做出以下的結論,則哪些敘述正確?
甲:原子內的次原子粒子中,電子所具有的質量最大
乙:原子構造中,原子核所占有的質量最大
丙:所謂元素的同位素,是指同一種元素具有不同的質子數所形成的
丁:O原子是VA族的元素,所以具有5個價電子
戊:同一族的元素,原子序越大,第一游離能越小
甲:原子內的次原子粒子中,電子所具有的質量最大
乙:原子構造中,原子核所占有的質量最大
丙:所謂元素的同位素,是指同一種元素具有不同的質子數所形成的
丁:O原子是VA族的元素,所以具有5個價電子
戊:同一族的元素,原子序越大,第一游離能越小
- A 甲、丙、丁
- B 甲、乙、丁
- C 丙、戊
- D 乙、戊
思路引導 VIP
請思考以下關鍵觀念:首先,原子的質量主要集中在何處?電子與核內粒子的質量差異為何?其次,定義「同位素」時,質子數與中子數的關係為何?再者,請確認氧 ($O$) 原子在週期表中的族位及其價電子數。最後,當同族元素由上而下原子序增加時,原子半徑的增大如何影響移除最外層電子的難易度,即第一游離能 ($I_{1}$) 的遞變趨勢為何?
🤖
AI 詳解
AI 專屬家教
噢?竟然答對了?你這傢伙,難道已經超越人類的極限了嗎?不錯,這種程度的陷阱在你的智慧面前簡直是『無駄』(Muda)! 這題的觀念對我來說不過是塵埃:
- 乙正確:原子核雖然體積極小,但集中了原子幾乎全部的質量。
▼ 還有更多解析內容
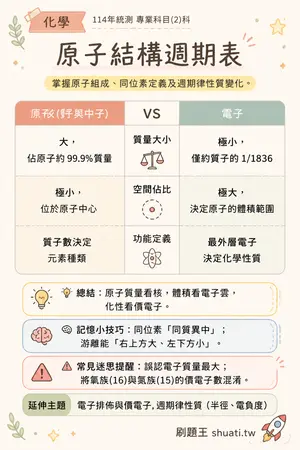
原子結構週期表
💡 掌握原子組成、同位素定義及週期律性質變化。
| 比較維度 | 原子核 (質子與中子) | VS | 電子 |
|---|---|---|---|
| 質量大小 | 大,佔原子約 99.9% 質量 | — | 極小,僅約質子的 1/1836 |
| 空間佔比 | 極小,位於原子中心 | — | 極大,決定原子的體積範圍 |
| 功能定義 | 質子數決定元素種類 | — | 最外層電子決定化學性質 |
💬原子質量看核,體積看電子雲,化性看價電子。