分科測驗
111年
化學
第 17 題
📖 題組:
16-17 題為題組 有甲、乙、丙、丁、戊、己等六個前三週期的元素,其相關的性質如表 3 所示。
16-17 題為題組 有甲、乙、丙、丁、戊、己等六個前三週期的元素,其相關的性質如表 3 所示。
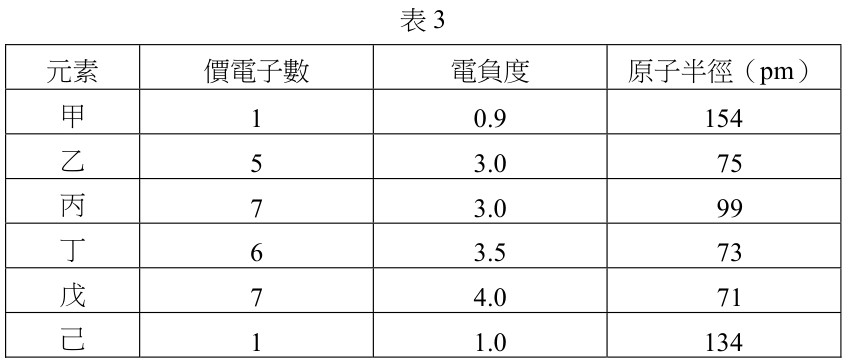
此六元素彼此之間可形成不同的化合物,下列相關化合物的敘述哪些正確?
- A 甲與丙可形成離子化合物
- B 乙與丁可形成多種化合物
- C 丁與戊形成的分子化合物中,丁的氧化數可為 -1
- D 乙與丙形成的分子化合物,其分子形狀為平面三角形
- E 甲與丁可形成離子化合物,其中丁的氧化數可為 -1或 -2
思路引導 VIP
如果我們先不看選項,單純觀察表格:請試著利用「價電子數」來猜測甲~己分別是哪一族的元素?接著,根據「電負度」的大小(例如小於 $1.0$ 與大於 $3.0$),你能分辨出誰是金屬、誰是非金屬嗎?這會如何決定它們相遇時,會形成離子鍵還是共價鍵呢?
🤖
AI 詳解
AI 專屬家教
🎉 表現得太棒了!
老師要大力肯定你的化學直覺與推理能力!你精準地判斷出正確選項。從表格的價電子與電負度,可推斷甲的電負度僅 $0.9$(為金屬 $\text{Na}$),丙的電負度為 $3.0$ 且價電子為 $7$(為非金屬 $\text{Cl}$)。兩者電負度差異大,結合必定形成離子化合物($\text{NaCl}$),你的基礎觀念非常紮實!
⚠️ 注意:本題為官方公告之爭議題
▼ 還有更多解析內容