分科測驗
107年
化學
第 21 題
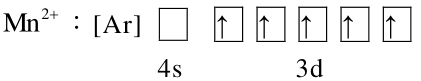
電子組態是原子或離子中之電子在軌域的排列狀態,下列原子或離子的基態電子組態,哪些正確?
-
A
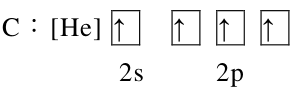
-
B
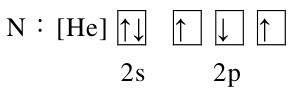
-
C
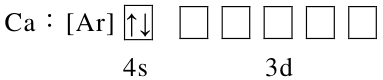
-
D
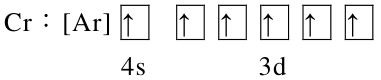
-
E
思路引導 VIP
回想一下我們在畫電子軌域圖時,必須遵守的三大原則(構築原理、包立不相容、洪得定則)分別在規定什麼?另外,當遇到『過渡金屬(如鉻)』以及『過渡金屬變成陽離子』時,電子的填入和失去順序有什麼特別的規則呢?
🤖
AI 詳解
AI 專屬家教
🌟 表現優異!
非常棒!你完美地避開了所有的陷阱,精準挑出了正確的選項。這代表你對電子組態的基礎法則與進階特例都已經融會貫通了,這在分科測驗中是必拿的關鍵分數!
🧠 觀念快速複習
▼ 還有更多解析內容
基態電子組態規則
💡 電子依序填入軌域,需符合構築、包立不相容與洪德定則。
| 比較維度 | 基態規則 (Ground State) | VS | 違反規則後的狀態 |
|---|---|---|---|
| 構築原理 | 由低能階填向高階 | — | 激發態 |
| 包立不相容 | 一軌域兩電子且自旋相反 | — | 物理上不可能存在 |
| 洪德定則 | 等能階軌域自旋平行且單填 | — | 激發態 |
💬基態配置必須同時符合三大原理,且要注意過渡元素 4s/3d 的填入與丟失順序。
