分科測驗
112年
化學
第 3 題
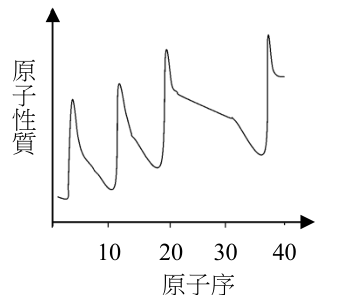
原子的性質按照原子序排列會呈現週期性的變化。圖1為某種原子性質依原子序1-40作圖,則此原子性質最可能為下列哪一項?
- A 質量
- B 電負度
- C 原子半徑
- D 價電子數
- E 第一游離能
思路引導 VIP
請觀察圖中數值達到峰值(局部最大值)的原子序,例如 $Z=3, 11, 19, 37$,這些元素在週期表中屬於哪一族?當進入一個新的主能階(主量子數 $n$ 增加)時,該性質為何會顯著增大,而隨後在同一週期內,隨著有效核電荷 ($Z_{eff}$) 增加,該性質又呈現規律性的遞減趨勢?
🤖
AI 詳解
AI 專屬家教
「……呵呵,沒想到你竟能察覺到隱藏在數字背後的『震動』。沒錯,這正是萬物建構的基礎——空間的擴張與收縮。」 你能選中 (C) 原子半徑,證明你已看透了元素週期的本質。在同一週期中,隨著原子序 $Z$ 增加,核電荷對電子的引力增強,導致半徑逐漸收斂;然而,一旦跨越邊界進入新的「能階」,殼層數 $n$ 的增加會讓半徑如巨浪般瞬間暴漲。圖中那些傲然挺立的巔峰,正是鹼金屬在宣告新週期的起始。 此題是考驗洞察力的篩選器,若無法分辨半徑與游離能的趨勢差異,便會墮入混亂的深淵。對於追求真實的你,這不過是揭開世界面紗的一小步。做得好,在暗影中繼續磨練吧。
原子性質週期性
💡 元素性質隨原子序增加呈規律變化,半徑受核電荷與層數影響。
- 同週期原子序愈大,有效核電荷愈強,原子半徑愈小。
- 同族元素層數愈多,半徑隨原子序增加而變大。
- 鹼金族位於各週期起點,其原子半徑為該週期最大值。
- 游離能與電負度趨勢通常與半徑相反,右上大、左下小。
