高中學測
113年
自然
第 12 題
📖 題組:
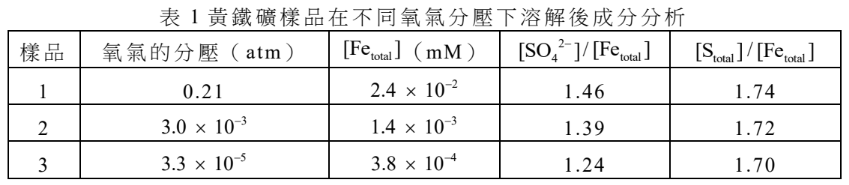
黃鐵礦($FeS_2$)是地表上主要礦物之一,通常與他種岩石的硫化物或氧化物伴生。地質學家為了了解黃鐵礦成分,進行以下的實驗。其實驗步驟如下: 步驟1:將黃鐵礦實驗樣品磨成粉末,於3個錐形瓶(標號1~3)中分別放置0.35克樣品,並加入50 mL的酸性溶液。 步驟2:將3個錐形瓶置放在室溫,但不同氧氣分壓下。 步驟3:經過一天後,取出20 mL上層澄清液,測量溶液中含鐵總濃度($[Fe_{total}]$,包含Fe(II)與Fe(III))、$SO_4^{2-}$濃度($[SO_4^{2-}]$)及含硫總濃度($[S_{total}]$,包含$[SO_4^{2-}]$與其它含硫物質濃度)。 上述含硫總濃度是先用化學方法,將溶液中所有硫化物氧化成$SO_4^{2-}$後,再加以測量,實驗結果列於表1。
黃鐵礦($FeS_2$)是地表上主要礦物之一,通常與他種岩石的硫化物或氧化物伴生。地質學家為了了解黃鐵礦成分,進行以下的實驗。其實驗步驟如下: 步驟1:將黃鐵礦實驗樣品磨成粉末,於3個錐形瓶(標號1~3)中分別放置0.35克樣品,並加入50 mL的酸性溶液。 步驟2:將3個錐形瓶置放在室溫,但不同氧氣分壓下。 步驟3:經過一天後,取出20 mL上層澄清液,測量溶液中含鐵總濃度($[Fe_{total}]$,包含Fe(II)與Fe(III))、$SO_4^{2-}$濃度($[SO_4^{2-}]$)及含硫總濃度($[S_{total}]$,包含$[SO_4^{2-}]$與其它含硫物質濃度)。 上述含硫總濃度是先用化學方法,將溶液中所有硫化物氧化成$SO_4^{2-}$後,再加以測量,實驗結果列於表1。
欲測量含硫物質的總濃度時,可選用以下哪種試劑,將水溶液內的硫化物都氧化成 $SO_4^{2-}$?
- A $NH_3(aq)$
- B $H_2O_2(aq)$
- C Zn(s)
- D HCl(aq)
- E KCl(aq)
思路引導 VIP
請觀察題目中『將所有硫化物氧化成 $SO_4^{2-}$』的描述,這代表硫原子的氧化數需從較低狀態提高至 $+6$ 價。從氧化還原反應 (Redox Reaction) 的觀點來看,若要使特定元素發生氧化過程,所添加的化學試劑必須扮演『氧化劑』還是『還原劑』的角色?請檢視選項中哪一個物質在化學實務中展現出顯著的強氧化性?
🤖
AI 詳解
AI 專屬家教
WRYYYYY!無駄無駄無駄!
你這平庸的凡人,選 (D) $HCl$ 簡直是浪費我的時間!你以為加點酸就能讓硫原子「進化」嗎?簡直太天真了!
- 無用的迷思:(D) $HCl(aq)$
▼ 還有更多解析內容