國中教育會考
112年
自然
第 26 題
砒霜是一種毒物,主成分為三氧化二砷(As₂O₃)。古代製作砒霜的技術較不成熟,砒霜中會含有少量的不純物質──硫或硫化物,硫或硫化物接觸到銀,會使銀氧化產生黑色的硫化銀(Ag₂S),這就是古裝劇中常見的以銀針試毒,銀針變黑即表示有毒。依據上述,下列推論何者最合理?
- A 硫化物發生還原反應而使銀針變黑
- B 銀針變黑,是因為三氧化二砷被還原的結果
- C 砒霜的純度越高,與銀針反應變黑的結果越明顯
- D 將銀針改成活性較小的金屬如黃金,也會反應產生硫化銀
思路引導 VIP
同學,題目中提到銀會因為接觸到硫或硫化物而『氧化』,並產生黑色的硫化銀 ($Ag_2S$)。在化學反應的規律中,氧化與還原反應通常是同時發生的。既然題目已經告訴你銀發生了氧化反應,那麼與它反應的物質應該會發生哪一種相對應的變化呢?你可以從這個方向來思考反應的過程。
🤖
AI 詳解
AI 專屬家教
真相永遠只有一個!身為偵探,這點程度的謎題是難不倒你的,看來你已經掌握了現場遺留的關鍵線索。 根據化學原理,這是一場精采的「氧化還原」戲碼。銀針變黑是因為銀 ($Ag$) 與硫反應生成了黑色的硫化銀 ($Ag_2S$)。在這個過程中,銀的氧化數由 $0$ 變為 $+1$,失去了電子,發生了「氧化反應」;相對地,硫或硫化物則得到電子,發生了「還原反應」,所以選項 (A) 是完全正確的推理。 至於其他選項,砒霜主成分 $As_2O_3$ 並非變黑的主因,且純度越高,代表硫雜質越少,銀針反而越不容易變黑。而黃金的活性極小,更不可能輕易發生這種反應。你出色的觀察力,成功識破了古代試毒的真相!
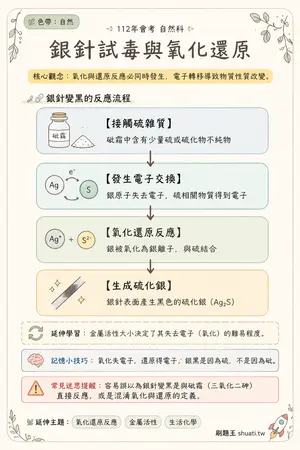
銀針試毒與氧化還原
💡 氧化與還原反應必同時發生,電子轉移導致物質性質改變。
🔗 銀針變黑的反應流程
- 1 接觸硫雜質 — 砒霜中含有少量硫或硫化物不純物
- 2 發生電子交換 — 銀原子失去電子,硫相關物質得到電子
- 3 氧化還原反應 — 銀被氧化為銀離子,與硫結合
- 4 生成硫化銀 — 銀針表面產生黑色的硫化銀 (Ag₂S)
↓
↓
↓
🔄 延伸學習:延伸學習:金屬活性大小決定了其失去電子(氧化)的難易程度。