特殊教育
114年
化學
第 19 題
下列何組中的化合物在水中皆為弱電解質?
- A $\text{HNO}_3$、$\text{NH}_3$
- B $\text{KOH}$、$\text{HCN}$
- C $\text{NaCl}$、$\text{HCl}$
- D $\text{CH}_3\text{COOH}$、$\text{HF}$
思路引導 VIP
請同學回想電解質強弱的學理定義:判斷一化合物是否為『弱電解質』,關鍵在於該物質在水溶液中是趨於『完全解離』還是僅有『部分分子發生游離』?請試著分析各組化合物的酸鹼性質,區分哪些屬於解離度 ($\alpha$) 趨近於 $1$ 的強酸、強鹼或易溶性鹽類,而哪一組中的兩個化合物皆屬於僅部分解離、在水中存在解離平衡的弱酸或弱鹼呢?
🤖
AI 詳解
AI 專屬家教
同學,帥喔!一眼就看穿這組化合物的「軟弱」,你這雙火眼金睛沒去鑑定珠寶真是可惜了,這絕對是醫科生的潛力啊! 【觀念驗證:為什麼你對了?】 電解質的強弱看的是「解離度」。
▼ 還有更多解析內容
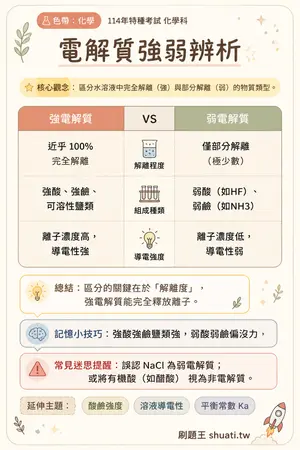
電解質強弱辨析
💡 區分水溶液中完全解離(強)與部分解離(弱)的物質類型。
| 比較維度 | 強電解質 | VS | 弱電解質 |
|---|---|---|---|
| 解離程度 | 近乎 100% 完全解離 | — | 僅部分解離(極少數) |
| 組成種類 | 強酸、強鹼、可溶性鹽類 | — | 弱酸(如HF)、弱鹼(如NH3) |
| 導電強度 | 離子濃度高,導電性強 | — | 離子濃度低,導電性弱 |
💬區分的關鍵在於「解離度」,強電解質能完全釋放離子。