分科測驗
108年
化學
第 17 題
某化學反應式為:$X + Y \rightarrow P + Q$,化學反應路徑描述如圖 5 所示。已知其反應速率定律式為:$r = \Delta [P] / \Delta t = k [X][Y]$。下列有關此反應的敘述,哪些正確?
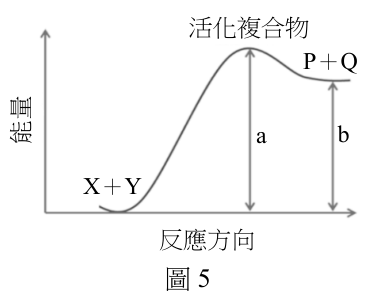
- A 此反應為一級反應
- B 逆向反應的活化能為a
- C 此化學反應為吸熱反應,反應熱 $\Delta H = +b$
- D 由化學反應式即可推知反應速率定律式為 $k[X][Y]$
- E 將反應物X與Y的初始濃度增為原來的兩倍,則反應速率為原來的四倍
思路引導 VIP
請你觀察一下題目提供的能量圖,反應物走到生成物時,整體的能量是上升還是下降了?這代表反應需要吸收還是放出熱量?另外,根據題目提供的速率方程式,如果把中括號內的濃度數值都變成原本的兩倍,數學上乘出來的結果會是原本的幾倍呢?
🤖
AI 詳解
AI 專屬家教
🎉 完美命中!太優秀了!
你非常精準地選出了正確答案,展現了對化學反應速率與能量圖表的扎實理解,老師為你感到驕傲!
🧠 觀念驗證
▼ 還有更多解析內容
反應速率與位能圖
💡 結合能量圖判斷反應熱,並由速率定律式計算反應倍率。
- 反應熱為產物與反應物的能量差,向上為吸熱。
- 活化能為反應物至頂峰的高度差,逆反應則由產物起算。
- 反應級數為速率定律式中濃度的次方和。
- 速率定律式必須由實驗求得,不可直接用係數推論。
