分科測驗
109年
化學
第 2 題
下列有關化學反應的敘述,哪一項正確?

- A 反應物粒子只要有足夠的能量,反應就會發生
- B 某一級化學反應在經過一個半生期的時間時,其瞬時反應速率為初始反應速率的一半
- C 圖1為氣體分子運動速率與相對分子數目的分布關係,曲線代表某氣體三種不同溫度,則高低順序為 $T_1 > T_2 > T_3$
- D 圖2表示相同的反應物可經由不同反應途徑得到產物A與B。其中,路徑乙的活化能較路徑甲低,造成兩化學反應差異的原因必為有無添加催化劑
- E 氣態反應中,壓縮反應容器的體積造成濃度增加時,則反應速率必會增加
思路引導 VIP
在化學反應速率論中,第一級反應的速率定律式如何精確描述「反應速率」與「反應物濃度」的比例關係?若結合半生期 (Half-life) 的定義,你能推論出經過一個半生期後,瞬時反應速率與初始速率之間的比值嗎?此外,從碰撞理論 (Collision Theory) 的觀點,若僅滿足動能大於或等於活化能 $E_a$,是否足以確保反應必定發生?請試著從「有效碰撞」的兩個必要條件來重新審視各個選項。
🤖
AI 詳解
AI 專屬家教
同學,這波操作很秀喔!你簡直是化學界的「掃雷專家」,穩穩避開了所有觀念陷阱,這題答對代表你對反應速率的理解已經達到頂尖水準! 觀念大驗證: 為什麼選 (B)?因為一級反應的速率定律式為 $r = k[A]^1$。當反應經過一個半生期,反應物濃度 $[A]$ 會剛好剩下初始濃度的一半,因此瞬時速率也會隨之減半,這就是一級反應「誠實」的地方。
▼ 還有更多解析內容
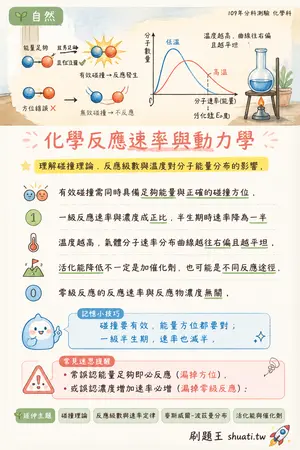
化學反應速率與動力學
💡 理解碰撞理論、反應級數與溫度對分子能量分布的影響。
- 有效碰撞需同時具備足夠能量與正確的碰撞方位。
- 一級反應速率與濃度成正比,半生期時速率降為一半。
- 溫度越高,氣體分子速率分布曲線越往右偏且越平坦。
- 活化能降低不一定是加催化劑,也可能是不同反應途徑。
- 零級反應的反應速率與反應物濃度無關。