分科測驗
108年
化學
第 6 題
📖 題組:
6-7為題組 做完秒錶反應後,為了要同學探究實驗過程中的試劑與其化學反應,張老師又用一個燒杯,演示了一組實驗。簡要過程如下:取一個盛有去離子水 100 毫升的大燒杯,放置於攪拌器上,使燒杯內的水穩定攪拌,然後滴入碘酒,使溶液呈現黃褐色。 ①加入X試劑,黃褐色褪去,溶液呈現無色。 ②加入雙氧水,黃褐色復現。 ③加入Y試劑,黃褐色褪去,溶液呈現無色。 ④加入鹽酸溶液,黃褐色復現。 其流程如右圖,①②③④為反應過程序號,依據實驗回答 6-7 題:
6-7為題組 做完秒錶反應後,為了要同學探究實驗過程中的試劑與其化學反應,張老師又用一個燒杯,演示了一組實驗。簡要過程如下:取一個盛有去離子水 100 毫升的大燒杯,放置於攪拌器上,使燒杯內的水穩定攪拌,然後滴入碘酒,使溶液呈現黃褐色。 ①加入X試劑,黃褐色褪去,溶液呈現無色。 ②加入雙氧水,黃褐色復現。 ③加入Y試劑,黃褐色褪去,溶液呈現無色。 ④加入鹽酸溶液,黃褐色復現。 其流程如右圖,①②③④為反應過程序號,依據實驗回答 6-7 題:
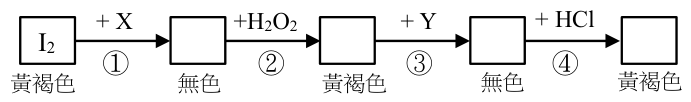
在①的步驟中,加入的試劑 X 是什麼?
- A HCl
- B $H_2SO_3$
- C NaOH
- D $H_2O_2$
- E $I_2$
思路引導 VIP
觀察步驟①,溶液從代表碘分子 ($I_2$) 的黃褐色變成了無色,你覺得碘的氧化數是變大還是變小了?為了促成這樣的改變,我們應該從選項中挑選具有什麼化學性質的試劑呢?
🤖
AI 詳解
AI 專屬家教
🌟 老師點評與肯定
太棒了!你非常精準地抓住了秒錶反應的核心觀念,這顯示你對氧化還原現象的判斷相當熟練,邏輯非常清晰,值得大大的肯定!
🔬 觀念驗證
▼ 還有更多解析內容
碘的氧化還原與顏色
💡 透過氧化還原使碘分子與碘離子互換並觀察顏色變化。
🔗 碘的顏色轉化與化學反應鏈
- 1 還原褪色 — 碘分子被亞硫酸還原成無色碘離子
- 2 氧化復色 — 碘離子被雙氧水氧化回黃褐色碘分子
- 3 動力學應用 — 利用澱粉當指示劑可精確計時反應速率
↓
↓
🔄 延伸學習:延伸學習:秒錶反應中反應物濃度與溫度的影響
