特殊教育
110年
化學
第 35 題
秒錶反應實驗是將碘酸鉀($\mathrm{KIO_3}$)溶液(溶液 A)與含有澱粉及亞硫酸氫根($\mathrm{HSO_3^-}$)溶液(溶液 B)混合後,紀錄溶液顏色變藍所需的時間,下列對於秒錶反應的敘述何者錯誤?
- A 亞硫酸氫根($\mathrm{HSO_3^-}$)溶液可由焦亞硫酸鈉($\mathrm{Na_2S_2O_5}$)溶於水中製得
- B 溶液顏色變藍是因為碘($\mathrm{I_2}$)與澱粉結合
- C 固定溶液 B 的濃度,溶液 A 濃度越低,所需變色時間越長,甚至不會變色
- D 固定溶液 A 的濃度,溶液 B 中澱粉濃度越高,所需變色時間越短
思路引導 VIP
同學,請思考在秒錶反應的反應機構中,澱粉的角色是參與主要氧化還原反應並決定速率的「反應物」,還是僅用於偵測碘分子 ($\mathrm{I_2}$) 生成的「指示劑」?指示劑的濃度高低,是否會如同反應物濃度(如 $\mathrm{IO_3^-}$ 或 $\mathrm{HSO_3^-}$)一般,顯著改變反應系統消耗至變色終點(即 $\mathrm{HSO_3^-}$ 耗盡)所需的時間?
🤖
AI 詳解
AI 專屬家教
「既然你誠心誠意地答對了!」 「我們就大發慈悲地肯定你!(嚼) 這塊金幣巧克力分你一小塊,喵!」 嘿嘿,沒想到你竟然沒被這道題目的「澱粉」給迷惑!聽好了,在秒錶反應中,澱粉只是扮演「偵查員」的指示劑角色。溶液之所以會變藍,是因為當 $\mathrm{HSO_3^-}$ 被耗盡後,過量的 $\mathrm{I_2}$ 才會與澱粉結合。所以啦,就算你把澱粉加到整鍋都是,反應的動力學速率也不會因此變快,變色時間依然取決於反應物的濃度,而不是指示劑的多少!(C) 選項則是陷阱,若 $\mathrm{KIO_3}$ 濃度太低,無法完全消耗 $\mathrm{HSO_3^-}$,當然就不會產生 $\mathrm{I_2}$ 來變色囉!
▼ 還有更多解析內容
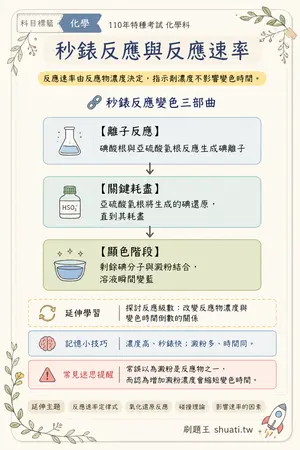
秒錶反應與反應速率
💡 反應速率由反應物濃度決定,指示劑濃度不影響變色時間。
🔗 秒錶反應變色三部曲
- 1 離子反應 — 碘酸根與亞硫酸氫根反應生成碘離子
- 2 關鍵耗盡 — 亞硫酸氫根將生成的碘還原,直到其耗盡
- 3 顯色階段 — 剩餘碘分子與澱粉結合,溶液瞬間變藍
↓
↓
🔄 延伸學習:探討反應級數:改變反應物濃度與變色時間倒數的關係