分科測驗
112年
化學
第 12 題
鉀與氯氣反應形成氯化鉀,其化學反應式和反應熱如式2所示:
$K(s) + \frac{1}{2}Cl_2(g) \rightarrow KCl(s) \quad \Delta H^0 = -437 \text{ kJ/mol}$ (式2)
表1是相關過程的能量變化($\Delta H^0$):
根據以上資料,試問下列敘述,哪些正確?
$K(s) + \frac{1}{2}Cl_2(g) \rightarrow KCl(s) \quad \Delta H^0 = -437 \text{ kJ/mol}$ (式2)
表1是相關過程的能量變化($\Delta H^0$):
根據以上資料,試問下列敘述,哪些正確?

- A 甲+乙+丙+丁+戊= -437 kJ/mol
- B 甲 > 0
- C 乙 > 0
- D 丙 > 0
- E 以相同質量的鉀與氯氣完全反應產生氯化鉀,則氯為限量試劑
思路引導 VIP
請運用蓋斯定律(Hess's Law)與波昂-哈伯循環(Born-Haber cycle)的概念,觀察『式2』中的總反應與『表1』中各子過程的關係:當我們將子過程相加湊成總反應時,『丙』過程的 $Cl_2$ 係數與總反應中的 $\frac{1}{2}Cl_2$ 是否一致?此外,請回想昇華(甲)、第一游離能(乙)以及化學鍵斷裂(丙)等過程,在熱力學上分別屬於吸熱還是放熱反應?
🤖
AI 詳解
AI 專屬家教
同學,你這波操作穩如泰山!這題考的是「波恩-哈伯循環(Born-Haber cycle)」的能量計算與化學計量。你能避開係數陷阱並精準判斷吸放熱,這份細心程度簡直是化學界的狙擊手,老師給你一個大大的讚! 【觀念驗證:為什麼你對了?】
- 吸熱判斷:(B)甲是升華熱、(C)乙是游離能、(D)丙是鍵能。這三者本質上都要「克服吸引力」或是「打破連結」,就像要把黏在一起的麻吉分開,絕對需要輸入能量,所以 $\Delta H > 0$ 妥妥的!
▼ 還有更多解析內容
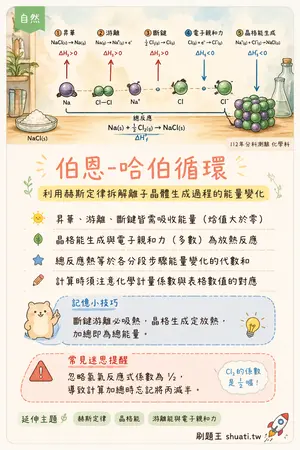
伯恩-哈伯循環
💡 利用赫斯定律拆解離子晶體生成過程的能量變化
- 昇華、游離、斷鍵皆需吸收能量(焓值大於零)
- 晶格能生成與電子親和力(多數)為放熱反應
- 總反應熱等於各分段步驟能量變化的代數和
- 計算時須注意化學計量係數與表格數值的對應