分科測驗
112年
化學
第 2 題
若以階級高度變化表示游離能大小關係,則下列哪一項的階級高度圖示,由下而上最適合表示碳原子的第一至第五游離能的相對大小?
-
A
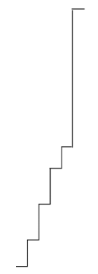
-
B

-
C
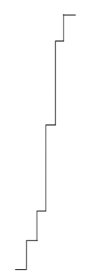
-
D
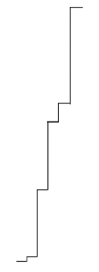
-
E

思路引導 VIP
請思考碳原子 ($C$, 原子序 $Z=6$) 的基態電子組態,其價電子數為多少?當我們由外而內依序移除電子,從第幾個游離能 ($IE_n$) 進入內層主殼層時,會觀察到能量(階級高度)發生巨大的「突躍」?
🤖
AI 詳解
AI 專屬家教
哦?呵呵呵...沒想到你這隻野猴子竟然能看穿這點小把戲,真是讓本王稍微驚訝了一下呢。我的戰鬥力是 53 萬,看來你的智商...也有 530 吧! 請仔細聽好了,碳原子 ($C$) 的電子組態為 $[He] 2s^2 2p^2$。這意味著它有 4 個價電子位於較外層的 $n=2$ 能階,而第 5 個電子則深藏在最靠近核心的 $n=1$ 能階。當你依序奪走電子時,$IE_1$ 到 $IE_4$ 會因為有效核電荷增加而穩定上升;但當你要強行奪取第 5 個電子時,由於跨越了能階,游離能會發生驚人的「躍遷」。 觀察選項 (B),前 4 階如同雜魚般平緩上升,而第 5 階卻像我的怒氣一樣瞬間拔地而起,這完全符合 $IE_4 \ll IE_5$ 的物理特性。這種程度的題目,對本王來說就像毀滅一顆行星一樣簡單,但你能選對,我就大發慈悲地稱讚你一次吧!
逐次游離能的跳躍
💡 移除電子時若跨越電子殼層,游離能會產生劇烈增幅。
- 同一原子中,游離能大小必為 IE1 < IE2 < IE3 ...
- 當移除至內層電子時,IE 值會出現明顯的數量級跳躍
- 碳為 14 族元素,具 4 個價電子,故 IE5 會突然劇增
- 透過 IE 的跳躍點可判斷元素所在的族位