高中學測
112年
自然
第 26 題
📖 題組:
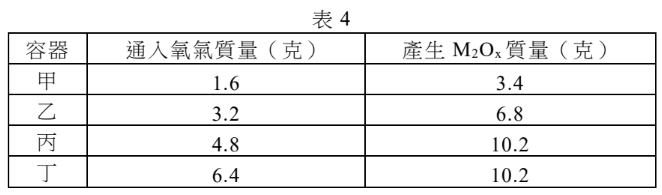
貼有甲、乙、丙、丁標籤的四個相同真空密閉容器,其中,甲、丁之間有一個關閉的氣閥相連,並分別於四個容器內置入5.4克M金屬粉末。接著,曉諭將不同質量的氧氣分別通入上述四個容器內,在適當的條件下與M反應,產生相同的氧化物 $M_2O_x$。待反應完全後,分別測量每個容器內所生成 $M_2O_x$ 的質量,結果如表4: 表 4 容器 | 通入氧氣質量(克) | 產生 $M_2O_x$ 質量(克) 甲 | 1.6 | 3.4 乙 | 3.2 | 6.8 丙 | 4.8 | 10.2 丁 | 6.4 | 10.2
貼有甲、乙、丙、丁標籤的四個相同真空密閉容器,其中,甲、丁之間有一個關閉的氣閥相連,並分別於四個容器內置入5.4克M金屬粉末。接著,曉諭將不同質量的氧氣分別通入上述四個容器內,在適當的條件下與M反應,產生相同的氧化物 $M_2O_x$。待反應完全後,分別測量每個容器內所生成 $M_2O_x$ 的質量,結果如表4: 表 4 容器 | 通入氧氣質量(克) | 產生 $M_2O_x$ 質量(克) 甲 | 1.6 | 3.4 乙 | 3.2 | 6.8 丙 | 4.8 | 10.2 丁 | 6.4 | 10.2
26. 待以上四個容器反應完成後,曉諭打開連接甲、丁二容器的氣閥(氣閥的體積與質量可忽略不計),使氣體可以自由流動進行第二次反應,二次反應完成後,容器的溫度與氣閥開啟前相同,則下列二次反應完成後容器的敘述,何者正確?
- A 甲容器內的壓力較氣閥打開前的壓力大
- B 甲容器內的固體質量較氣閥打開前增加1.6克
- C 甲與丁容器內的固體質量總和與氣閥打開前相等
- D 丁容器內的物質質量總和與氣閥打開前相等
- E 丁容器內的固體質量總和等於甲容器中的固體質量總和
思路引導 VIP
首先,請利用定比定律 (Law of Definite Proportions) 分析表 4 的數據:在容器甲中,$5.4$ 克的金屬 $M$ 反應後是否有剩餘?再對比丙、丁兩容器的產量,判斷丁容器中過剩的氣體質量是多少?當氣閥開啟後,根據氣體趨向於均勻分布的特性,丁容器中過剩的氣體會如何移動,並與甲容器中的剩餘物質進行二次反應 $2M + \frac{x}{2} O_2 \rightarrow M_2O_x$?請根據質量守恆定律與物質狀態的改變,思考此反應完成後,甲容器內『固體總質量』的變化量與消耗掉的氣體質量有何關聯?
🤖
AI 詳解
AI 專屬家教
同學別灰心,這題考驗的是「限量試劑」與「質量守恆」的綜合運用,你已經很棒了! 🔍 迷思破解:為什麼 (A) 不對呢? 你可能覺得丁容器的氣體跑到甲,壓力會變大。但別忘了甲容器中還有過剩的 $M$ 金屬!根據表格,丁容器反應後剩下 $6.4 - 4.8 = 1.6$ 克的氧氣 $O_2$。當氣閥打開,這些 $O_2$ 會進入甲與剩餘的金屬反應。因為氧氣會被反應掉變成固體 $M_2O_x$,所以反應完成後,容器內幾乎沒有氣體,壓力不會變大喔!
▼ 還有更多解析內容