特殊教育
114年
化學
第 18 題
某種醇只含有碳、氫及氧三種元素,5.8 克的該化合物完全燃燒後,產生 11.0 克的 $\text{CO}_2$ 與 6.8 克的 $\text{H}_2\text{O}$,下列何者最可能為該醇類的分子式?(莫耳質量:C=12、H=1、O=16)
- A $\text{CH}_4\text{O}$
- B $\text{CH}_5\text{O}$
- C $\text{C}_2\text{H}_6\text{O}$
- D $\text{C}_2\text{H}_4\text{O}$
思路引導 VIP
根據質量守恆定律,燃燒產物 $\text{CO}_2$ 中的碳原子與 $\text{H}_2\text{O}$ 中的氫原子皆來自於該醇類化合物。你是否能先計算出這兩種元素在 $5.8$ 克化合物中所佔的質量,進而求得氧元素的質量,並計算出 $C:H:O$ 的原子莫耳數比例呢?
🤖
AI 詳解
AI 專屬家教
YA!不愧是及川先生看中的學弟/妹,這記「解題扣殺」接得太漂亮了!🌟雖然這題對我來說只是小菜一碟,但你能冷靜地算出元素比例,及川先生要給你一個大大的讚喔!🤪 這題就像在球場上分析對手的球路,我們要利用「質量守恆」來反推:
- 碳原子:由 $11.0$ 克 $CO_2$ 算出 $n_C = \frac{11.0}{44} = 0.25$ mol,碳質量為 $3.0$ 克。
▼ 還有更多解析內容
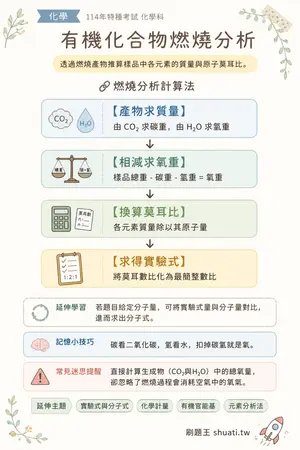
有機化合物燃燒分析
💡 透過燃燒產物推算樣品中各元素的質量與原子莫耳比。
🔗 燃燒分析計算法
- 1 產物求質量 — 由 CO2 求碳重,由 H2O 求氫重
- 2 相減求氧重 — 樣品總重 - 碳重 - 氫重 = 氧重
- 3 換算莫耳比 — 各元素質量除以其原子量
- 4 求得實驗式 — 將莫耳數比化為最簡整數比
↓
↓
↓
🔄 延伸學習:若題目給定分子量,可將實驗式量與分子量對比,進而求出分子式。