分科測驗
107年
化學
第 5 題
📖 題組:
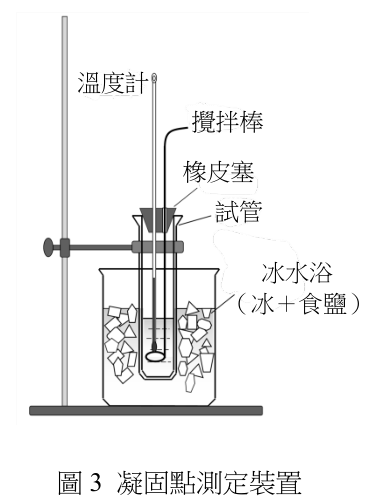
5-6題為題組 賈同學在實驗室發現一瓶標籤已脫落的白色粉末狀試藥,為了探究此未知化合物為何,於是依照實驗手冊中[凝固點下降的測定]實驗之步驟做了兩組凝固點測定,以求得此未知物的分子量。 [實驗一] 水的凝固點測定:將純水倒入已置於冷劑(食鹽加冰塊)的試管中(圖 3),並立即攪拌,每 30 秒記錄水的溫度。 [實驗二] 未知化合物溶液的凝固點測定:秤取 9.75 克的白色粉末,溶於 50 毫升的純水,攪拌使樣品完全溶解,再如實驗一的步驟將此化合物溶液倒入試管中,每 30 秒記錄溶液的溫度。 賈同學分別將兩組實驗的數據,以時間(分)為橫軸,溫度(℃)為縱軸作圖,得到如圖 4 的冷卻曲線。
5-6題為題組 賈同學在實驗室發現一瓶標籤已脫落的白色粉末狀試藥,為了探究此未知化合物為何,於是依照實驗手冊中[凝固點下降的測定]實驗之步驟做了兩組凝固點測定,以求得此未知物的分子量。 [實驗一] 水的凝固點測定:將純水倒入已置於冷劑(食鹽加冰塊)的試管中(圖 3),並立即攪拌,每 30 秒記錄水的溫度。 [實驗二] 未知化合物溶液的凝固點測定:秤取 9.75 克的白色粉末,溶於 50 毫升的純水,攪拌使樣品完全溶解,再如實驗一的步驟將此化合物溶液倒入試管中,每 30 秒記錄溶液的溫度。 賈同學分別將兩組實驗的數據,以時間(分)為橫軸,溫度(℃)為縱軸作圖,得到如圖 4 的冷卻曲線。
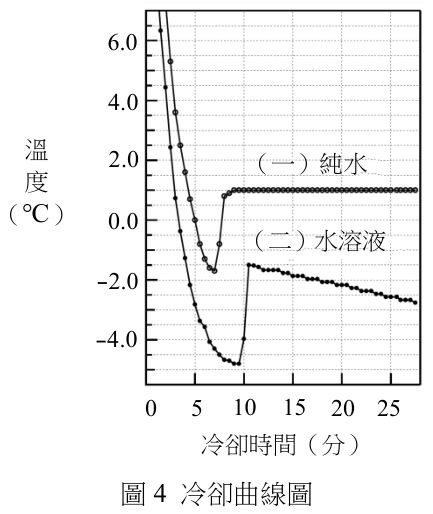
試問此化合物的水溶液凝固點下降度數(℃)應最接近下列哪一選項?
- A 0.7
- B 1.4
- C 2.0
- D 2.8
- E 4.8
思路引導 VIP
觀察圖中的冷卻曲線,當液體發生『過冷現象』導致溫度急速下降後,溫度會突然回升。請試著找出『純水』與『水溶液』回溫後的『最高溫度』分別對應到縱軸的幾度?接著想想看,即便溫度計有誤差,我們該如何利用這兩個數字來求出真正的『下降度數』呢?
凝固點下降測定
💡 藉由冷卻曲線求出凝固點下降量,進而推算溶質分子量。
- 由冷卻曲線回溫後的最高點判定為起始凝固點
- 公式:ΔTf = i * Kf * m,注意電解質的 i 值
- 重量莫耳濃度 m 的分母須使用溶劑的「公斤」數
- ΔTf 為純溶劑與溶液凝固點之差值,必為正值
