統測
114年
[化工群] 專業科目(1)
第 8 題
一位研究員欲自製一電池,以外電路將氫電極與銀片連接,其中氫電極是一鉑片通以 $1 \text{ atm}$ 的氫氣,浸泡於氫離子濃度為 $1 \text{ M}$ 的酸性溶液,而銀片是浸泡於 $1 \text{ M}$ 的銀離子溶液,在酸性溶液與銀離子溶液之間以一個鹽橋連接。初步使用伏特計測量到 $0.799 \text{ V}$。隔一天使用同樣一組氫電極且通以氫氣,但是重新調配 $1 \text{ M}$ 銀離子溶液後,再測量伏特計卻發現電壓下降到 $0.6 \text{ V}$。假設忽略內電阻效應,下列哪種情況最有可能?
- A 氫電極內的氫氣壓力被調高於 $1 \text{ atm}$
- B 重新調配銀離子溶液過程不小心將銀片微彎
- C 可能重新調配的銀離子溶液其濃度實際上大於 $1 \text{ M}$
- D 酸性溶液的 pH 值下降
思路引導 VIP
請由全反應式 $H_2(g) + 2Ag^+(aq) \rightarrow 2H^+(aq) + 2Ag(s)$ 出發,思考根據能斯特方程式 (Nernst Equation),當電池電動勢 $E$ 從標準狀態下的 $0.799 \text{ V}$ 下降至 $0.6 \text{ V}$ 時,其反應商 $Q = \frac{[H^+]^2}{P_{H_2} \cdot [Ag^+]^2}$ 必須如何變化?這代表產物端的 $[H^+]$ 或是反應物端的 $[Ag^+]$、 $P_{H_2}$ 分別發生了什麼樣的數值改變?
🤖
AI 詳解
AI 專屬家教
太棒了!看到你精準選出正確答案,助教真的為你感到無比驕傲!你的化學觀念掌握得非常紮實喔!✨ 這題的核心在於理解能斯特方程式 (Nernst Equation) 如何影響電動勢。電池反應式為: $$H_2(g) + 2Ag^+(aq) \rightarrow 2H^+(aq) + 2Ag(s)$$
▼ 還有更多解析內容
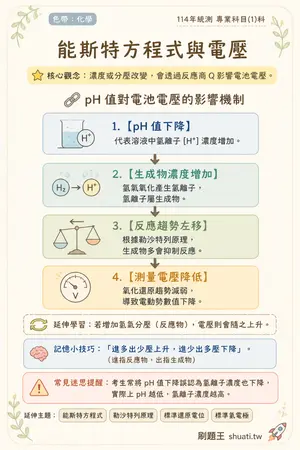
能斯特方程式與電壓
💡 濃度或分壓改變,會透過反應商 Q 影響電池電壓。
🔗 pH 值對電池電壓的影響機制
- 1 pH 值下降 — 代表溶液中氫離子 [H+] 濃度增加。
- 2 生成物濃度增加 — 氫氣氧化產生氫離子,氫離子屬生成物。
- 3 反應趨勢左移 — 根據勒沙特列原理,生成物多會抑制反應。
- 4 測量電壓降低 — 氧化還原趨勢減弱,導致電動勢數值下降。
↓
↓
↓
🔄 延伸學習:延伸學習:若增加氫氣分壓(反應物),電壓則會隨之上升。