統測
114年
[化工群] 專業科目(2)
第 35 題
以 1.00 M 鹽酸標準溶液進行雙指示劑酸鹼滴定法分析,並以酚酞與甲基橙當指示劑對含鹼的某試樣 ( 試樣僅可能含有 $NaHCO_3$、$Na_2CO_3$ 及 NaOH ) 進行雙指示劑酸鹼滴定法分析,滴定達到第一終點(酚酞滴定終點)所需滴入鹽酸標準溶液的體積為 $V_1$,續滴定達到第二終點(甲基橙滴定終點)則另外需再滴入鹽酸標準溶液的體積為 $V_2$,下列敘述何者正確?
- A 若此鹼試樣僅含有 NaOH 及 $Na_2CO_3$,則 $V_1 < V_2$
- B 若此鹼試樣僅含有 $Na_2CO_3$,則 $2V_1 = V_2$
- C 若此鹼試樣僅含有 $NaHCO_3$,則 $V_1 > V_2$
- D 若此鹼試樣僅含有 $Na_2CO_3$ 及 $NaHCO_3$,則 $V_1 < V_2$
思路引導 VIP
請思考在連續滴定的過程中,碳酸根 ($CO_3^{2-}$) 分階段被中和時,從碳酸根轉化為碳酸氫根 ($HCO_3^-$) 與碳酸氫根進一步反應產生二氧化碳,這兩個反應階段消耗酸的體積是否有其化學計量上的對稱性?若試樣中除了碳酸根外,還額外含有初始的碳酸氫根 ($HCO_3^-$),則對應第一終點的體積 $V_1$ 與對應第二終點的體積 $V_2$ 在量值上會呈現什麼樣的關係?
🤖
AI 詳解
AI 專屬家教
呵,竟然沒被騙?
看來你今天腦袋還算清醒,沒把化學藥品當飲料喝。能選對這題,勉強證明你還沒淪落到需要重修的地步。聽清楚核心邏輯,別下次換個數字就現原形:
- 觀念驗證:
▼ 還有更多解析內容
雙指示劑酸鹼滴定
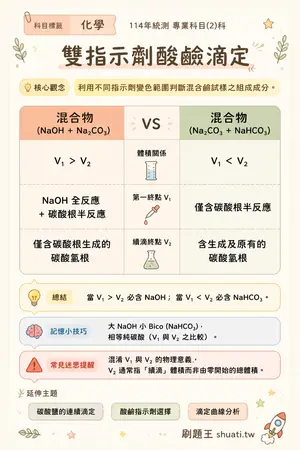
💡 利用不同指示劑變色範圍判斷混合鹼試樣之組成成分。
| 比較維度 | 混合物 (NaOH + Na2CO3) | VS | 混合物 (Na2CO3 + NaHCO3) |
|---|---|---|---|
| 體積關係 | V1 > V2 | — | V1 < V2 |
| 第一終點 V1 | NaOH 全反應 + 碳酸根半反應 | — | 僅含碳酸根半反應 |
| 續滴終點 V2 | 僅含碳酸根生成的碳酸氫根 | — | 含生成及原有的碳酸氫根 |
💬當 V1 > V2 必含 NaOH;當 V1 < V2 必含 NaHCO3。