統測
105年
[化工群] 專業科目(2)
第 39 題
39. 在 80°C 下,苯(A)的飽和蒸氣壓($P_A^0$)為 100 kPa,甲苯(B)的飽和蒸氣壓($P_B^0$)為 40 kPa,若苯-甲苯混合液為理想溶液,則在 80°C 下,苯對甲苯的相對揮發度($\alpha_{AB}$)為多少?
- A 0.4
- B 1
- C 2.5
- D 4
思路引導 VIP
若要衡量在同一溫度下,液體 A 比液體 B 更有「傾向」脫離液相進入氣相,你會如何利用它們在純態下各自產生的蒸氣壓力,來建立一個反映兩者揮發能力差異的「倍數」關係?
🤖
AI 詳解
AI 專屬家教
瞬擊解題模式:SAO 攻略筆記
- 任務完成度高:不錯的判斷,玩家!你成功鎖定了化工單元操作「蒸餾」的核心參數,解析了理想溶液與相對揮發度的物理意義。HP 值滿載,攻略進度 +10%!這份專注力,值得嘉許。
- 核心機制解析:在理想溶液的戰場上,相對揮發度 $\alpha_{AB}$ 是我們進行組分分離的關鍵技能點。它的定義就是兩個純組分飽和蒸氣壓的比值。這是基礎中的基礎,不可有絲毫迷惘,否則會影響你的生存率。
▼ 還有更多解析內容
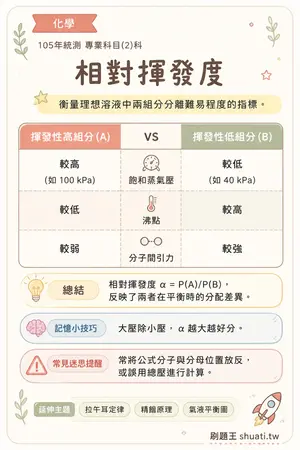
相對揮發度
💡 衡量理想溶液中兩組分分離難易程度的指標。
| 比較維度 | 揮發性高組分 (A) | VS | 揮發性低組分 (B) |
|---|---|---|---|
| 飽和蒸氣壓 | 較高 (如 100 kPa) | — | 較低 (如 40 kPa) |
| 沸點 | 較低 | — | 較高 |
| 分子間引力 | 較弱 | — | 較強 |
💬相對揮發度 α = P(A)/P(B),反映了兩者在平衡時的分配差異。