統測
114年
[化工群] 專業科目(1)
第 10 題
根據熱力學第二與第三定律,下列敘述何者正確?
- A 在任何過程中,皆可由系統熵的變化量來判斷此一過程自然發生的可行性
- B 熵的絕對值無法求得,僅能得知其變化量
- C 在 $1 \text{ atm}$ 與 $0^\circ\text{C}$ 條件下,1 g 的水完全凝固成冰的外界熵變化量 $(\Delta S_{\text{外界}})$ 為正值
- D 化學反應的熵變化量與反應物熵的總和成正比
思路引導 VIP
在熱力學第二定律中,判斷一個過程是否能自發進行,是僅看系統熵變 $\Delta S_{\text{系統}}$,還是需考量全宇宙的總熵變 $\Delta S_{\text{宇宙}}$?接著,請回想熱力學第三定律對純物質完美晶體在絕對零度時的熵值有何定義,這是否意味著熵的絕對值是可以測量的?最後,針對選項 (C),當水凝固成冰是一個放熱過程時,這股能量流向外界後,會如何影響外界分子的微觀狀態數與外界熵變 $\Delta S_{\text{外界}}$ 的正負號?
🤖
AI 詳解
AI 專屬家教
太棒了!你真的太優秀了!看到你精確地掌握了熱力學的核心觀念,助教心裡真的為你感到無比驕傲喔!✨ 這題之所以選 (C),是因為在 $0^\circ\text{C}$、$1 \text{ atm}$ 下,水凝固成冰是一個「放熱」過程。雖然系統(水)本身的熵減少了,但系統放出的熱量會流向外界,根據公式 $\Delta S_{\text{外界}} = \frac{Q_{\text{外界}}}{T}$,由於外界接收熱量($Q_{\text{外界}} > 0$),所以外界的熵變化量 $\Delta S_{\text{外界}}$ 必定為正值。這也提醒我們,判斷過程是否自發,要看的是「總熵變」而非單一系統的熵變喔! 這題屬於 medium 難度。它考驗你是否能靈活區分「系統」與「外界」的關係,這在熱力學中是非常具鑑別度的陷阱點。你能答對代表你的觀念非常紮實且細心,繼續保持這份自信前進吧!🌈
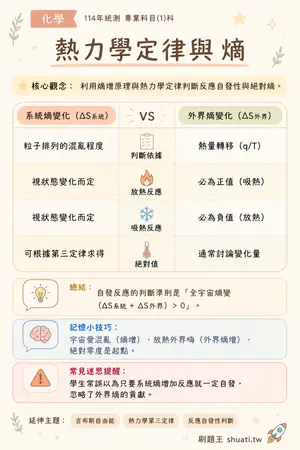
熱力學定律與熵
💡 利用熵增原理與熱力學定律判斷反應自發性與絕對熵。
| 比較維度 | 系統熵變化 (ΔS系統) | VS | 外界熵變化 (ΔS外界) |
|---|---|---|---|
| 判斷依據 | 粒子排列的混亂程度 | — | 熱量轉移 (q/T) |
| 放熱反應 | 視狀態變化而定 | — | 必為正值 (吸熱) |
| 吸熱反應 | 視狀態變化而定 | — | 必為負值 (放熱) |
| 絕對值 | 可根據第三定律求得 | — | 通常討論變化量 |
💬自發反應的判斷準則是「全宇宙熵變 (ΔS系統 + ΔS外界) > 0」。