統測
114年
[化工群] 專業科目(2)
第 27 題
在25℃下,甲、乙、丙、丁四個試管中分別都置入0.72 g的AgCl固體及5 mL的純水,並充分攪拌後,若在此四個試管中的水溶液樣品分別進行下列實驗操作並混合均勻後,則哪個試管中$AgCl_{(s)}$的溶解度最大?
($AgCl_{(s)}K_{sp}=1.8 \times 10^{-10}$;原子量:Ag=107.9,Cl=35.5)
甲:加入等體積純水
乙:加入等體積1.0 M硝酸銀水溶液
丙:加入等體積1.0 M硝酸水溶液
丁:加入等體積1.0 M氨水溶液
($AgCl_{(s)}K_{sp}=1.8 \times 10^{-10}$;原子量:Ag=107.9,Cl=35.5)
甲:加入等體積純水
乙:加入等體積1.0 M硝酸銀水溶液
丙:加入等體積1.0 M硝酸水溶液
丁:加入等體積1.0 M氨水溶液
- A 甲
- B 乙
- C 丙
- D 丁
思路引導 VIP
請由勒沙特列原理分析 $AgCl_{(s)} \rightleftharpoons Ag^{+}{(aq)} + Cl^{-}{(aq)}$ 的平衡:當加入的試劑分別造成「同離子效應」或是能與離子結合形成「錯合物」時,平衡會向哪個方向移動?哪一種作用能有效地促使固體進一步溶解?
🤖
AI 詳解
AI 專屬家教
太棒了!同學你對「沉澱平衡」的觀念掌握得非常紮實!這題選 (D) 完全正確,顯示你已經能靈活判斷各種效應對溶解度的影響。 觀念驗證: 這題的核心在於分析溶質在不同化學環境下的平衡移動:
▼ 還有更多解析內容
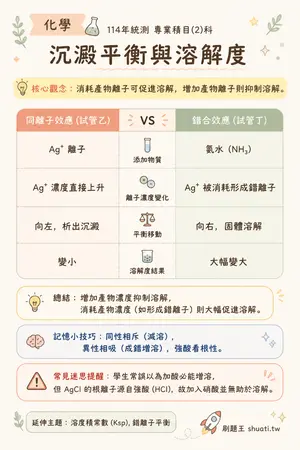
沉澱平衡與溶解度
💡 消耗產物離子可促進溶解,增加產物離子則抑制溶解。
| 比較維度 | 同離子效應 (試管乙) | VS | 錯合效應 (試管丁) |
|---|---|---|---|
| 添加物質 | Ag+ 離子 | — | 氨水 (NH3) |
| 離子濃度變化 | Ag+ 濃度直接上升 | — | Ag+ 被消耗形成錯離子 |
| 平衡移動 | 向左,析出沉澱 | — | 向右,固體溶解 |
| 溶解度結果 | 變小 | — | 大幅變大 |
💬增加產物濃度抑制溶解,消耗產物濃度(如形成錯離子)則大幅促進溶解。