分科測驗
114年
化學
第 23 題
📖 題組:
在混合溶液中,不同種類分子的分子間作用力差距,會影響溶液偏離理想性質的幅度。圖 10 是在 1 大氣壓下,環己烷-乙醇混合溶液所測得的沸點對乙醇莫耳分率數值(X)的曲線。回答下列問題:
在混合溶液中,不同種類分子的分子間作用力差距,會影響溶液偏離理想性質的幅度。圖 10 是在 1 大氣壓下,環己烷-乙醇混合溶液所測得的沸點對乙醇莫耳分率數值(X)的曲線。回答下列問題:
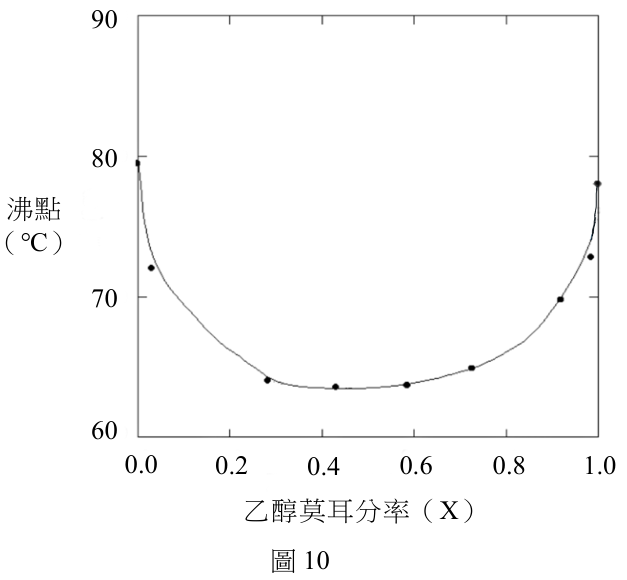
關於環己烷-乙醇混合溶液的敘述,哪些正確?(多選)
- A X=0.5 的環己烷-乙醇混合溶液沸點約為 64 ℃
- B 將 0.5 L 環己烷與 0.5 L 乙醇混合後,溶液總體積大於 1.0 L
- C 環己烷與乙醇混合為放熱反應
- D 環己烷分子間作用力大於乙醇分子間作用力
- E 環己烷分子與乙醇分子之間主要以偶極-偶極力互相吸引
思路引導 VIP
觀察圖中的曲線變化,混合溶液的沸點整體上比原來的純物質更高還是更低?這暗示著它們混合後,分子變得更容易逃逸成氣體,還是更難逃逸?由此推論,異種分子之間的吸引力比混合前的同種分子強還是弱呢?
💬 其他同學也在問
1
怎麼看出來是正偏差的
非理想溶液與正偏差
💡 溶質與溶劑作用力弱於原純物質,形成正偏差。
- 正偏差:混合後分子間作用力變弱,總蒸氣壓升高。
- 能量與體積:混合過程為吸熱,混合後總體積大於兩者之和。
- 沸點表現:正偏差溶液之沸點會低於各純物質組成分。
- 力與性質:非極性與極性分子混合常導致作用力變弱。
