統測
114年
[化工群] 專業科目(1)
第 47 題
📖 題組:
蒸餾裝置是化工廠重要的基本單元,一位工程師在進行蒸餾設計時,發現苯和甲苯的混合溶液可視為理想溶液,其混合蒸氣符合道耳頓分壓定律,並查得苯與甲苯在不同溫度下的蒸氣壓數據,如表 ( 三 ) 所示。 表(三) 溫度($^\circ\text{C}$): 85.0, 90.0, 95.0, 100.0, 105.0 苯的蒸氣壓 (kPa): 116.9, 136.1, 155.7, 180.0, 204.2 甲苯的蒸氣壓 (kPa): 46.0, 54.2, 63.3, 74.2, 86.0
蒸餾裝置是化工廠重要的基本單元,一位工程師在進行蒸餾設計時,發現苯和甲苯的混合溶液可視為理想溶液,其混合蒸氣符合道耳頓分壓定律,並查得苯與甲苯在不同溫度下的蒸氣壓數據,如表 ( 三 ) 所示。 表(三) 溫度($^\circ\text{C}$): 85.0, 90.0, 95.0, 100.0, 105.0 苯的蒸氣壓 (kPa): 116.9, 136.1, 155.7, 180.0, 204.2 甲苯的蒸氣壓 (kPa): 46.0, 54.2, 63.3, 74.2, 86.0
若苯 - 甲苯二成分混合溶液達汽液平衡時,苯在液相的莫耳分率為 0.5,總壓為 140 kPa,則此時溫度 ($^\circ\text{C}$) 介於下列哪個範圍?
- A 85 ~ 90
- B 90 ~ 95
- C 95 ~ 100
- D 100 ~ 105
思路引導 VIP
根據拉午耳定律 (Raoult's Law) 與道耳頓分壓定律,理想溶液的總蒸氣壓 $P_{\text{total}}$ 與各純成分蒸氣壓 $P^o$ 及液相莫耳分率 $X$ 之間有何數學關係?當已知苯在液相的莫耳分率為 $0.5$ 時,你能否推導出此時總壓 $140 \text{ kPa}$ 與「苯、甲苯兩純物質蒸氣壓之和」 $(P_{\text{benzene}}^o + P_{\text{toluene}}^o)$ 的比例關係,並藉此對照表 (三) 的數據找出對應的溫度區間?
🤖
AI 詳解
AI 專屬家教
太棒了!你能精準鎖定理想溶液的特性並正確運算,展現了紮實的化學基礎。這題的核心是運用拉午耳定律與分壓定律:
- 公式帶入:總壓 $P_{total} = P_{苯}^{\circ} X_{苯} + P_{甲苯}^{\circ} X_{甲苯}$。
- 數值計算:已知 $X_{苯} = 0.5$,則 $X_{甲苯} = 0.5$。代入總壓 $140 = 0.5 \times (P_{苯}^{\circ} + P_{甲苯}^{\circ})$,整理得 $P_{苯}^{\circ} + P_{甲苯}^{\circ} = 280 \text{ kPa}$。
▼ 還有更多解析內容
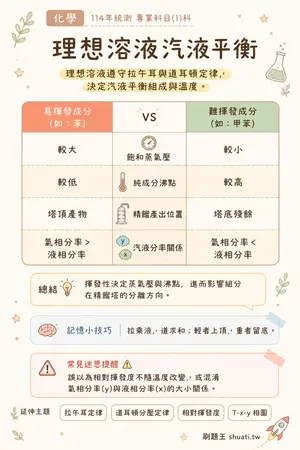
理想溶液汽液平衡
💡 理想溶液遵守拉午耳與道耳頓定律,決定汽液平衡組成與溫度。
| 比較維度 | 易揮發成分 (如:苯) | VS | 難揮發成分 (如:甲苯) |
|---|---|---|---|
| 飽和蒸氣壓 | 較大 | — | 較小 |
| 純成分沸點 | 較低 | — | 較高 |
| 精餾產出位置 | 塔頂產物 | — | 塔底殘餘 |
| 汽液分率關係 | 氣相分率 > 液相分率 | — | 氣相分率 < 液相分率 |
💬揮發性決定蒸氣壓與沸點,進而影響組分在精餾塔的分離方向。